Rev Med UAS
Rev Med UAS; Vol. 15 No. 4. Octubre-Diciembre 2025
ISSN 2007-8013
David Levaro-Loquio1,#, Aldo Arturo Reséndiz-Albor1,#, Rosa Adriana Jarillo-Luna 1,2, Germán Higuera-Martínez1, Munich Guevara-Rubio1, Maritza Tatiana Velásquez-Torres1, Judith Pacheco-Yépez1*
*Autor de correspondencia: Dr. Judith Pacheco Yépez
Escuela Superior de Medicina, Instituto Politécnico Nacional, Plan de San Luis S/N,
Casco de Santo Tomas, CP 11340, CDMX, México.
Email: jpachecoy@ipn.mx; Tel. +52 5557296300 ext 62743
#Estos autores han contribuido de igual forma en este trabajo
DOI http://dx.doi.org/10.28960/revmeduas.2007-8013.v15.n4.007
Texto Completo PDFRecibido 24 de junio 2025, aceptado 22 de octubre 2025
RESUMEN
El absceso hepático amibiano (AHA) ocasionado por Entamoeba histolytica (E. histolytica) ocurre debido a la liberación exacerbada de especies reactivas de oxígeno (EROs). Enzimas prooxidantes como la NADPH oxidasa (NOX) participa en la producción de EROs producidas por las células inmunitarias, como mecanismo de defensa, pero estas EROs también dañan a las células del hospedero. Trabajos in vitro han mostrado que el tratamiento con diversos inhibidores de la NOX, entre ellos la apocinina, han demostrado la disminución del daño celular inducido por E. histolytica. El objetivo de la presente revisión es explorar la modulación de enzimas prooxidantes como la NOX como una nueva estrategia en el tratamiento del AHA disminuyendo así el daño oxidativo y favoreciendo la resolución de la infección causada por E. histolytica.
Palabras clave: Entamoeba histolytica, Absceso Hepático Amibiano, Enzima NADPH oxidasa, modelo animal
ABSTRACT
The amebic liver abscess (ALA) caused by E. histolytica occurs due to the exacerbated release of reactive oxygen species (ROS). Pro-oxidant enzymes, such as NADPH oxidase (NOX) participates in the production of ROS produced by immune cells as a defense mechanism, but these ROS also damage host cells. In vitro work has shown that treatment with various NOX inhibitors, including apocynin, have demonstrated the decrease in cell damage induced by E. histolytica. This review aims to explore the modulation of pro-oxidant enzyme, such as NOX, as a new strategy for treating ALA. This plan would reduce oxidative damage and promote the resolution of E. histolytica caused infections.
Keywords: Entamoeba histolytica, Amebic Liver Abscess, NADPH oxidase enzyme, animal model
Introducción
Las infecciones parasitarias representan un gran problema de salud pública1,2, muchas especies de parásitos están asociados a enfermedades graves principalmente en poblaciones vulnerables con falta de acceso a servicios de salud y bajas condiciones de saneamiento o inmunodeprimidas3. Una de estas enfermedades parasitarias es la amibiasis, causada por el protozoario E. histolytica, protozoario patógeno causante de la amebiasis en humano. Aproximadamente, de 40 a 50 millones de personas en todo el mundo están infectadas con este parásito, y aproximadamente entre 40 000 y 100 000 pacientes infectados con E. histolytica mueren cada año en todo el mundo; por lo tanto, representa un importante problema de salud pública4. En México según datos de la Secretaría de Salud en años recientes (2020-2023), la incidencia de amibiasis en México es de aproximadamente 15 a 25 casos por cada 100,000 habitantes anuales5.
El fármaco de elección en el tratamiento de la amibiasis es el metronidazol, sin embargo algunas cepas de amibas han presentado resistencia a este fármaco2. Experimentalmente, en modelos animales se ha inducido el AHA7–9 en donde E. histolytica genera una reacción inflamatoria exacerbada, las células inmunes entran en contacto con los trofozoítos, son lisadas y liberan EROs, estas especies dañan tanto a la amiba como a las células del huésped incrementando el daño al parénquima hepático. Una de las enzimas prooxidantes que genera estas EROs es la NOX, la cual produce el anión superoxido (O2.-). Trabajos recientes han reportado que el uso de inhibidores de estas enzimas en modelos de AHA disminuyó el porcentaje del AHA10,11. Esta revisión explora mediante el uso de inhibidores de enzimas prooxidantes de enzimas como la NOX, la modulación en la producción de EROs las cuales favorecen el daño tisular en el AHA, utilizando a estas enzimas como blancos terapéuticos para impedir la evolución del AHA. En la presente revisión abordaremos la infección por E. histolytica, el desarrollo del AHA experimental, la generación de estrés oxidativo en el AHA, el papel de la NOX ante E. histolytica y el efecto de inhibidores de la NOX en algunas enfermedades y en el AHA.
Infección por E. histolytica
La infección por E. histolytica inicia cuando la forma infectiva, quistes, son ingeridos por el huésped a través de agua o alimentos contaminados, los quistes viajan a través del intestino delgado y llegan al íleon terminal, donde se produce el desenquistamiento y dan lugar al trofozoíto, la forma invasiva12,13. El trofozoíto es pleomórfico y móvil. E. histolytica puede invadir la mucosa intestinal ocasionando colitis amibiana o un daño más severo, como la disentería amibiana. Por otro lado, si el trofozoíto no invade la mucosa del intestino avanza por el colon y forma prequistes mononucleares para posteriormente formar la fase de quiste tetranucleado, este proceso finaliza cuando se forma la pared del quiste y es expulsado a través de la materia fecal al medio ambiente. En ocasiones el parásito invade vía sanguínea otros órganos, el más común es el hígado, provocando el AHA12,13.
AHA experimental
Experimentalmente, se ha estudiado detalladamente el desarrollo histopatológico del AHA, por medio de la inoculación de E. histolytica en el hígado de hámster (Mesocricetus auratus), un modelo susceptible a la amibiasis hepática7. En la fase aguda de la infección, a los 30 minutos se observa la dilatación de los sinusoides debido a la presencia de los trofozoítos, se observan en las ramas de la vena porta y en venas centrales del parénquima hepático, las células hepáticas no muestran cambios. A los 60 minutos de evolución del AHA, los trofozoítos con aspecto normal, se localizan en los sinusoides y rodeados de polimorfonucleares (PMNs). A las 3 horas post-inoculación se visualizan múltiples focos inflamatorios, estos focos presentan trofozoítos en posición central rodeados por células PMNs y los hepatocitos muestran núcleos alargados. A las 6 horas post-inoculación, el tamaño de los infiltrados inflamatorios se incrementa, obervando células mononucleres y PMNs; en la periferia de las lesiones se observan leucocitos lisados y el daño de los hepatocitos es evidente. A las 9 y 12 horas, el tamaño de los infiltrados inflamatorios y de las lesiones es mayor, los hepatocitos presentan un contorno irregular, también se visualizan áreas necróticas con células inmunitarias y hepatocitos lisados. En la fase crónica 24-48 horas post-inoculación, el hígado muestra lesiones irregulares, hay hepatocitos necróticos, leucocitos lisados, zonas hemorrágicas y áreas de isquemia; finalmente a los 7 días se observan extensas zonas de necrosis licuefactiva correspondientes a granulomas fusionados7.
Estos eventos en el AHA causan una respuesta inmune descontrolada y un incremento en la concentración de EROs y óxido nítrico (ON), lo cual correlaciona con el tamaño y la severidad de la lesión7. El daño hepático se debe a que los neutrófilos liberan EROs y ON como mecanismo de defensa contra E. histolytica, la acumulación de EROsS en el AHA incrementa la acción oxidativa provocando la peroxidación de fosfolípidos y proteínas afectando así la permeabilidad de la membrana en las células y provocando lisis en el sitio de infección14,15. Además se ha reportado la activación de monocitos en circulación los cuales liberan citocinas y EROs, el papel de las EROs en el desarrollo del AHA es importante y requiere una mayor investigación15–17.
Estrés oxidativo en el AHA
El estrés oxidativo es un desequilibrio en la formación de especies oxidantes y antioxidantes, donde se favorece la formación de especies oxidantes provocando un aumento de las EROs. Los neutrófilos, eosinófilos y macrófagos son una fuente de especies reactivas y son los principales contribuyentes de las EROs18–20. El estrés oxidativo es comúnmente asociado con varias enfermedades hepáticas incluyendo el AHA, en el modelo susceptible del hámster existe una inflamación descontrolada y un alto estrés oxidativo. E. histolytica dispone de diversos mecanismos de defensa que resultan eficaces contra este entorno tóxico sin embargo; los factores moleculares subyacentes responsables de la progresión del daño tisular siguen siendo en gran medida desconocidos21,22.
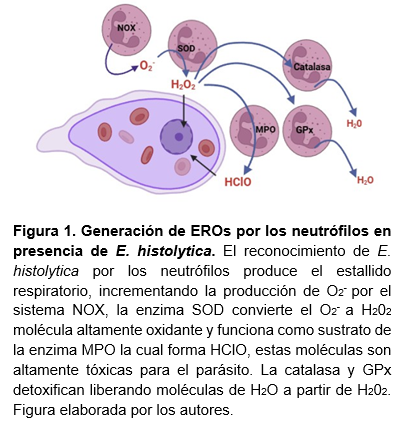
Como ya mencionamos la producción de EROs es importante en la defensa contra este parásito23–25, donde el papel del NOX es producir O2.-, para que posteriormente, actúe otra enzima llamada superóxido dismutasa (SOD) la cual convierte rápidamente el O2.- a peróxido de hidrogeno (H2O2) que también funciona como sustrato para otra enzima llamada mieloperoxidasa (MPO), que a partir del H2O2 cataliza la oxidación de dos iones de cloro produciendo ácido hipocloroso (HClO)26–28 (Figura 1).

Enzima NOX
La enzima NOX se encuentra en mamíferos y pertenece a una familia de enzimas (NOX 1-5 y oxidasa dual (DUOX 1, 2)29,30. Las diferencias más significativas entre estas enzimas son la expresión y su localización órgano-específica. Las EROs que provienen de la NOX modifican químicamente a moléculas relacionadas con la formación de hormonas y a la matriz extracelular, la defensa del hospedero y la señalización redox31. La actividad de la enzima NOX, consiste en transferir electrones de manera direccional desde el citosol hasta el O2 en la superficie externa de la membrana, el O2.- se libera extracelularmente cuando la NOX está en la superficie celular, pero cuando la actividad se localiza en las membranas internas como en los fagosomas se libera en las vesículas32. La actividad de las enzimas NOX es modulada directa o indirectamente por el calcio y afecta a todas las NOX, a excepción de la NOX4 que es constitutiva. La función biológica de las enzimas NOX es por tanto, la generación de EROs, por lo que esta enzima está implicada en el estallido respiratorio31,33.
Una célula puede tener una NOX activa en la membrana plasmática, proporcionando una actividad constante de oxidantes en la superficie celular34. Aunque todas las isoformas NOX comparten una homología estructural basada en un núcleo catalítico común compuesto por seis hélices transmembranales, un dominio deshidrogenasa (DH) que une el cofactor no covalente flavina (FAD) y al sustrato NADPH; los electrones pasan desde el NADPH hacia el FAD, y a los grupos hemo y finalmente de estos al O229. La enzima NOX en las células fagocíticas es de vital importancia para la eliminación de microrganismos y también forma parte importante de la cadena de transporte de electrones de la oxidasa microbicida de células fagocíticas junto con el citocromo b-245 el cual es un componente integral terminal de este sistema35.
En la eliminación de parásitos y otros microorganismos los neutrófilos son esenciales, desempeñando un papel importante en la regulación inflamatoria, estas células activan la enzima NOX2 necesaria para generar elevadas cantidades de O2- y desencadenan la activación de diferentes EROs36. Las EROs también inducen la muerte celular programada a través de la activación de las caspasas.
La enzima NOX2 está conformada por un conjunto de subunidades citosólicas (p40phox, p67phox, p47phox y Rac1) y dos subunidades transmembranales (gp91phox y p22phox) las cuales al recibir un estímulo la fracción p47 es fosforilada provocando el reclutamiento y ensamblaje de las otras subunidades a la fracción membranal y la activación del complejo enzimático permitiendo el transporte de electrones responsables de la reducción del O2 molecular en O2.-30,31,34. Es importante mencionar que la presencia de la enzima NOX2 se ha descrito en diversas enfermedades infecciosas como en ratones C57BL/6 infectados con Leishmania amazonensis, los roedores fueron inoculados con promastigotes metacíclicos en la dermis de la oreja de ratones silvestres W o ratones deficientes en gp91phox (gp91phox2/2) (subunidad necesaria para la activación de NOX2) con una infección de 1-16 semanas, mostraron que los ratones deficientes en la subunidad gp91 (gp91phox2/2) presentaban una patología más grave en las últimas fases de la infección; además se observó que las EROs derivadas de NOX2 controlaban la inflamación causada por Leishmania amazonensis mediando la apoptosis de neutrófilos inducida por la infección37.
Efecto de inhibidores de NOX
Se han reportado diversas moléculas que funcionan como inhibidores de la NOX; el cloruro de difenilenodonio (DPI), es una molécula lipofílica que inhibe de manera eficaz la producción de O2.- por la NOX de los neutrófilos, también inhibe la reducción dependiente de NADPH tanto del FAD como del Citocromo b24538. DPI es un inhibidor especifico de NOX2 el cual es ampliamente utilizado porque interactúa con la subunidad catalítica de NOX239, sin embargo esté presenta una elevada toxicidad y tiene una falta de especificidad a concentraciones micromolares por lo que su uso es limitado en aplicaciones clínicas y experimentales40,41.
Por su parte la 2-aminoethyl-benzenesulfonyl fluoride (AEBSF) es un inhibidor de serina proteasas que bloquea la producción de O2.- en macrófagos y también la activación de la enzima NOX, AEBSF interfiere con la interacción de la p47phox y/o la p67phox probablemente por modificación química del citocromo b55942. Sin embargo AEBSF no es un inhibidor directo de NOX, sino que actúa inhibiendo serina proteasas, se ha reportado que su efecto sobre la producción de EROs puede ser indirecto31.
También se ha demostrado el efecto inhibidor de un péptido antibacteriano endógeno rico en prolina-arginina llamado PR-39, este péptido inhibe la actividad de la NOX bloqueando el ensamblaje a través de interacciones con dominios de p47phox, PR-39 tiene múltiples funciones pues además de regular la producción de O2.- por la enzima NOX, limita el daño tisular durante la inflamación43. La síntesis y purificación de estos péptidos a escala industrial puede ser costosa, limitando su viabilidad comercial para ciertos usos44.
El camperol es un flavonoide de origen natural que ha sido identificado como un inhibidor de la enzima NOX, esta hidroxiflavona se une directamente a p47phox, la subunidad reguladora de NOX45. También se ha demostrado que la inhibición de NOX es un mecanismo que previene la producción de EROs46. En cuanto al efecto antioxidante del camperol, presenta un efecto en la disminución de EROs en interacciones de neutrófilos de hámster con trofozoítos de E.histolytica por 90 min47. Sin embargo, el uso de este fármaco ha mostrado diversas desventajas, su absorción es limitada en el tracto gastrointestinal, reduciendo su eficacia terapéutica por vía oral, es poco soluble en agua, lo que limita su biodisponibilidad y su aplicación terapéutica48,49.
La quercetina también es un flavonoide presente de forma natural en diversas plantas y se utiliza como suplemento nutricional debido a sus reconocidas propiedades antioxidantes y antiinflamatorias. Se ha demostrado recientemente que la quercetina induce la expresión de la enzima antioxidante hemo oxigenasa-1 (HO-1) en estudios tanto in vitro como in vivo. La actividad de HO-1 genera bilirrubina, un potente antioxidante capaz de neutralizar diversas EROs, lo que favorece la protección celular frente al estrés oxidativo asociado a NOX. Además, la quercetina puede inhibir directamente el ensamblaje y el proceso de activación de NOX50. Se han realizado diversos estudios sobre genotoxicidad y mutagenicidad a corto y largo plazo en animales y seres humanos en presencia de quercetina, donde se demostró en ensayos in vitro la mutagenicidad relacionada con las altas concentraciones del fármaco. Los resultados de los estudios in vitro demostraron sistemáticamente la mutagenicidad relacionada con la quercetina aún se discuten los mecanismos que conducen a la aparente mutagenicidad in vitro51.
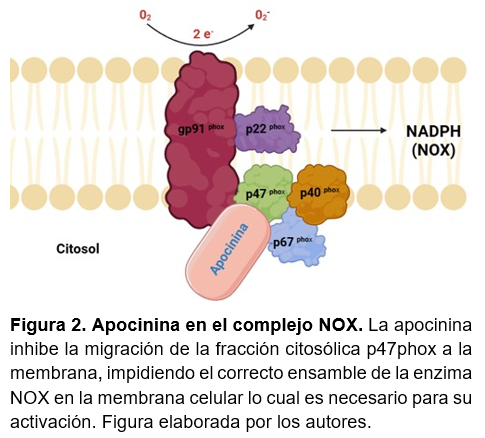
Por otro lado, la apocinina (4′-hidroxi-3′-metoxiacetofenona) es un extracto de la planta Picrorhiza kurroa, empleada en la medicina tradicional oriental para tratar enfermedades del hígado y es utilizada como agente antiinflamatorio y antioxidante52. La apocinina inhibe la activación de la enzima NOX debido a que reacciona con la subunidad citosólica p47 de la enzima lo que impide su ensamblaje, también inactiva los residuos sulfhidrilos esenciales para esta proteína53 (Figura 2).
El efecto antiinflamatorio y antioxidante de la apocinina ha sido reportado previamente por Oostwould y cols (2016) en ratones con enfermedad pulmonar y elevada inflamación donde al administrar apocinina, se redujo la inflamación en estos ratones54. En otro trabajo Horemans y cols en 2017 evaluaron el efecto de la apocinina en tejido intestinal infectado por Helicobacter pilori en jerbos, observando que la inhibición de la enzima NOX presente en los neutrófilos, regulo la producción de EROs las cuales producen daño tisular en el tejido infectado55.
En la búsqueda de la exploración del papel protector de la apocinina, El-Sawalhi y cols analizaron el efecto de la apocinina en ratas, las cuales presentaron cardiotoxicidad causada por la inyección de cisplatino56.
El cisplatino es un potente agente quimioterapéutico con amplia actividad antineoplásica, sin embargo presenta complicaciones cardiovasculares agudas tras el tratamiento57. En el trabajo de El-Sawalhi MM y Ahmed LA, se indujo cardiotoxicidad por medio de la inyección de cisplatino a una dosis de 7 mg/kg por vía intraperitoneal, y para evaluar el papel antioxidante de la apocinina, ésta fue administrada a 600 mg/L durante cinco días antes y después de la inyección de cisplatino. Transcurrido el tiempo sacrificaron a los animales y se extirparon los ventrículos para determinar la actividad de la NOX. Los resultados muestran un incremento del estrés oxidativo en el grupo tratado con cisplatino el cual está asociado al incremento en la actividad de la NOX. En tanto que en los animales que recibieron pretratamiento con apocinina disminuyo la actividad de la NOX comparada con el grupo tratado con cisplatino donde la actividad aumento. Los autores concluyeron que el pretratamiento con apocinina mejoró notablemente el estado del estrés oxidativo y mitigó la inflamación en estos animales56.
NOX y E. histolytica
Un estudio analizó el papel de la enzima NOX4 en la respuesta de células T Jurkat en presencia de E. histolytica. Las células fueron incubadas con el parásito durante 1 hora, lo que provocó un aumento significativo en la producción de EROs, en comparación con células mantenidas únicamente en medio de cultivo. La participación de NOX4 en este proceso se evaluó mediante dos estrategias experimentales, la primera fue la inhibición de NOX con DPI, donde observo que el pretratamiento redujo notablemente la generación de EROs inducida por el parásito y previno la fragmentación del ácido desoxirribonucleico (ADN) en las células huésped. La segunda estrategia fue el silenciamiento génico de NOX4 mediante el ácido ribonucleico pequeño de interferencia (siARN), donde la reducción de la expresión de NOX4 impidió tanto la producción de EROs como la fragmentación del ADN provocadas por E. histolytica. Estos resultados demuestran que NOX4 cumple un papel esencial en la generación de EROs y en la inducción de muerte celular en células T Jurkat tras su interacción con E. histolytica, destacando su relevancia en los mecanismos citotóxicos en la célula blanco mediados por este parásito58.
Mas recientemente, Lee y cols en 2023, investigaron la importancia de la NOX en la destrucción dependiente de EROs de hepatocitos inducida por los trofozoítos de E. histolytica, para ello incubaron células HepG2 con trofozoítos amibianos durante 1 hora, se reportó un incremento considerable de la fragmentación del ADN en comparación con células incubadas únicamente con el medio de cultivo, también demostraron una acumulación intracelular de EROs en las células HepG2 estimulada por los trofozoítos. Para analizar el papel de la enzima NOX, las células HepG2 fueron pretratadas con un inhibidor específico de NOX2 llamado GSK 2795039 el cual redujo la generación de EROs inducida por E. histolytica, por lo que estos resultados apoyan el papel de las EROs derivadas de NOX2 en la muerte de los hepatocitos inducidos por E. histolytica59.
NOX en el AHA
En modelos in vivo, Cortes y cols en 2019 analizaron el efecto de la apocinina en ratones BALB/c, un modelo resistente contra la amibiasis. Los animales fueron primero inmunizados con lisados amibianos y posteriormente tratados con apocinina 8 horas antes de la inoculación del parásito por vía intraperitoneal. Al sacrificio a las 6, 24 y 72 horas se demostró la eficacia de la apocinina debido a que el infiltrado inflamatorio estimulado por las amibas disminuyó considerablemente a estos tiempos11.
Recientemente se ha reportado el efecto de este fármaco en el modelo susceptible del hámster, a los animales se les indujo la formación del AHA. Los hámsteres se sacrificaron en la fase aguda a tiempos de 3, 6 y 12 horas post-inoculación con E. histolytica. La apocinina se administró a una dosis de 1.64 miligramos por cada 100 gramos de peso, la primera dosis fue administrada intraperitonealmente 8 horas antes de la inoculación de los trofozoítos en el hígado, se administró cada 8 horas, por lo que a las 3 horas solo se administró una dosis, a las 6 horas se administraron 2 dosis y a las 12 horas se aplicaron 3 dosis. Los autores reportaron una disminución en la progresión del AHA en todos los tiempos estudiados, se redujo el estrés oxidativo al aminorar la producción de O2.- demostrando que la administración de apocinina disminuye la actividad NOX, y reduce el infiltrado inflamatorio, además se observó que la apocinina daña de manera directa a los trofozoítos de E. histolytica, estos efectos favorecieron la resolución del AHA. El uso de este inhibidor de la NOX con capacidad antioxidante y antiinflamatoria evita el desarrollo del AHA en los hámsteres en la fase aguda del AHA10. Aunque se tienen resultados prometedores del efecto de la apocinina en el modelo susceptible se requiere explorar los beneficios de la apocinina en la fase crónica. Esta podría ser a futuro una nueva estrategia terapéutica para tratar el AHA, dado que, en el modelo susceptible, el bloqueo de la enzima NOX favorece la resolución del AHA. Estos trabajos previos muestran evidencias de la importancia de la NOX en la generación del daño tisular. El daño es inducido tanto por E. histolytica como por la respuesta de las células inflamatorias del huésped las cuales generan especies reactivas a partir de enzimas prooxidantes entre ellas la NOX, por lo que modular la actividad de esta enzima mediante el uso de inhibidores podría ser una estrategia novedosa en el tratamiento de la amibiasis hepática.
Conclusión
La regulación de la NOX es de vital importancia para reducir el estrés oxidativo mediante la disminución de la formación de EROs. Los inhibidores de NOX pueden modificar la expresión de la enzima, impedir el ensamblaje y la activación de los complejos NOX reduciendo por lo tanto el entorno oxidante en el AHA lo cual favorece la resolución de la lesión hepática amibiana. El uso de inhibidores de la NOX como la apocinina en modelos animales experimentales como terapias de tratamiento ha sido exitoso. A futuro será relevante evaluar inhibidores selectivos y específicos de las isoformas de la NOX para determinar los mecanismos que intervienen en el proceso patológico y en la respuesta inmunológica que monta el huésped ante E. histolytica. Estas estrategias innovadoras dirigidas en el uso de inhibidores de la NOX podrían ganar mayor impulso en el uso de nuevos tratamientos los cuales podrían mostrar resultados prometedores en la resolución de enfermedades infecciosas.
Agradecimientos
Agradecimiento del apoyo recibido por SAPPI IPN Proyecto Transdisciplinario 2341: 20250870, 20250872
Referencias