Rev Med UAS
Rev Med UAS; Vol. 15 No. 3. Julio-Septiembre 2025
ISSN 2007-8013
Ana Isabel Nevárez-Cota1, Brisceya Arce-Bojórquez1, Erik Rene Lizárraga-Verdugo1, Alexis Montero-Garcia1, Gabriela Álvarez-Osuna1
*Autor de correspondencia: Ana Isabel Nevárez Cota
Eustaquio Buelna. No. 91 Col. Gabriel Leyva. C. P. 80030. Culiacán, Sinaloa. Correo: an_nc92@hotmail.com
DOI http://dx.doi.org/10.28960/revmeduas.2007-8013.v15.n3.002
Texto Completo PDFRecibido 03 de febrero 2025, aceptado 16 de junio 2025
RESUMEN
Materias y métodos: Se trata de un estudio de concordancia diagnóstica, observacional, comparativo y retrospectivo, donde se comparó la relación de mortalidad existente entre la saturación venosa central de oxígeno y la escala APACHE II en pacientes con sepsis abdominal. Para este estudio se incluyeron los expedientes clínicos de pacientes con diagnóstico de sepsis abdominal, quienes fueron evaluados mediantes la escala APACHE II y, a su vez, se realizó la determinación de saturación venosa central de oxígeno, posteriormente, se evaluó la concordancia diagnóstica entre estas dos herramientas. Resultados: El estudio reveló que tanto la SvCO2 como la escala APACHE II son indicadores predictivos significativos de la mortalidad en pacientes con sepsis abdominal. Se observó que los pacientes que no sobrevivieron tendían a tener valores más bajos de SvCO2 y puntajes más altos en la escala APACHE II, lo que refleja una peor oxigenación, mala perfusión tisular y una mayor gravedad del estado clínico.
Palabras claves: Sepsis, choque séptico, perfusión tisular, saturación venosa central.
ABSTRACT
Materials and methods: In this observational, comparative and retrospective diagnostic agreement study, the mortality relationship between central venous oxygen saturation and the APACHE II score was compared in patients with abdominal sepsis. For this study, the clinical records of abdominals sepsis were included, who were evaluated using the APACHE II score and, in turn, the determination of central venous oxygen saturation was carried out, subsequently, the diagnostic agreement between these was evaluated two tools. Results and conclusions: The study revealed that both SvCO2 and the APACHE II score are significant predictive indicators of mor-tality in patients with abdominal sepsis. It was observed that patients who did not survive tended to have lower SvCO2 values and higher APACHE II score scores, reflecting worse oxygenation and greater severity of the clinical condition.
Key words: Sepsis, septic shock, tissue perfusion, central venous saturation.
Introducción
La sepsis es considerada en todo el mundo como una de las causas de mortalidad con mayor impacto. Se trata de una respuesta inflamatoria sistémica del cuerpo ante una infección, que de no ser tratada a tiempo puede evolucionar a choque séptico y posteriormente a falla orgánica múltiple.
La mortalidad asociada a sepsis y choque séptico puede variar según diversos factores, por mencionar algunos ejemplos; la gravedad de la infección, la edad del paciente, y la prontitud en establecer el tratamiento adecuado. Según el Instituto Nacional de Estadística y Geografía (INEGI), en 2018, la septicemia ocupó el lugar número 16 en mortalidad, con 4959 defunciones, de las cuales, 2506 fueron hombres y 2453 fueron mujeres. Se estima que cuando hay evolución a choque séptico, la mortalidad alcanza hasta un 27-59%. Esto implica estancias intrahospitalarias prolongadas y elevados costos en atención médica, lo que representa un importante impacto para los sistemas de salud pública. Es fundamental enfocarse en prevenir, promover la detección temprana y el tratamiento adecuado con prontitud de ésta condición.1
Entre los orígenes de mayor incidencia en sepsis podemos mencionar el origen abdominal en un 47% (peritonitis, apendicitis complicada, entre otros), seguidos del origen pulmonar en un 33%, y de tejidos blandos en 8%.1,2
En el 2016, el tercer consenso internacional para la definición de sepsis y choque séptico
(Sepsis-3) definió sepsis como la disfunción de órganos que pone en peligro la vida, causada por una respuesta exagerada del huésped a la infección. Esta última actualización asume que sepsis conlleva disfunción orgánica, eliminando lo que anteriormente se conocía como sepsis grave. Los criterios que se mencionan para definir choque séptico son:3
1. Hipotensión arterial; presión arterial media (PAM) < 65 mmHg, a pesar de un tratamiento adecuado a base de reanimación hídrica.
2. Necesidad de aminas vasopresoras; hipotensión persistente a pesar de la adecuada reanimación hídrica, donde se requiriere la administración de medicamentos vasopresores, noradrenalina se primera línea, para mantener la presión arterial en rangos aceptables. Como segunda opción se considera vasopresina o adrenalina.
3. Elevación de ácido láctico > 2 mmol/l.
Sepsis y choque séptico son padecimientos dependientes entre sí, para que un paciente evolucione de sepsis a un estado de choque séptico están involucrados diversos factores tanto del huésped como del microorganismo patógeno, pero sobre todo, una respuesta inadecuada, excesiva e incontrolada por parte del huésped. Otros factores de riesgo son la liberación desregularizada de mediadores inflamatorios, vasodilatación sistémica marcada, hipercoagulabilidad, e hipoperfusión tisular.4
Durante la evolución de sepsis a choque séptico pueden observarse tres fases, misma que podrán presentarse de manera simultánea durante su desarrollo:5
• Fase inicial: en esta fase los mecanismos compensatorios son activados para evitar el estado de choque mediante los reflejos de barorreceptores, la liberación de catecolaminas, secreción de hormona antidiurética y la estimulación del sistema nervioso autónomo simpático. En consecuencia, se produce elevación de la frecuencia cardiaca, vasoconstricción periférica y retención de líquidos.
• Fase progresiva: sucede al persistir durante un periodo de tiempo. Ésta fase se caracteriza por hipoperfusión, activación de la respiración intracelular anaerobia con producción de ácido láctico y, en consecuencia, acidosis metabólica, vasodilatación, empeoramiento del gasto cardiaco, lesiones anóxicas de las células endoteliales y coagulación intravascular diseminada (CID).
• Fase irreversible: la evolución de lo anterior mencionado, provoca la extravasación de enzimas lisosómicas, la producción de óxido nítrico aumenta, la función cardiaca se deteriora, y posteriormente puede presentarse isquemia intestinal, insuficiencia renal, disfunción multiorgánica y, finalmente, la muerte.
La sepsis abdominal se presenta por la respuesta sistémica del cuerpo frente a una infección localizada inicialmente en órganos de la cavidad abdominal, como el epiplón y el peritoneo. Esta infección puede ocurrir en varias formas; en primer lugar, la infección puede ocurrir de manera espontánea, especialmente en pacientes con ascitis, en quienes la infección se propaga a través del torrente sanguíneo hasta afectar la cavidad peritoneal. En segundo lugar, la infección puede ser introducida directamente en la cavidad peritoneal, lo que es más común en pacientes bajo tratamiento con diálisis peritoneal; durante este procedimiento, se utiliza un catéter para administrar una solución en la cavidad peritoneal, esto aumenta el riesgo de infección en el sitio de colocación del catéter. Otra forma de infección peritoneal ocurre cuando hay una ruptura en la integridad del tracto gastrointestinal, y la salida del contenido intestinal hacia la cavidad peritoneal ocasiona foco infeccioso. Esta presentación se conoce como peritonitis secundaria y puede manifestarse como una infección generalizada del peritoneo o como un absceso localizado.6
Por otro lado, la peritonitis terciaria describe una infección persistente o recurrente que ocurre principalmente en pacientes críticos que tienen antecedentes de peritonitis secundaria. Esto puede suceder cuando el sistema inmunológico del paciente está comprometido o después del fracaso de la terapia antimicrobiana inicial. En estos casos, puede producirse una sobreinfección por órganos resistentes, como bacilos gramnegativos u hongos.6
En de sepsis abdominal, los patógenos más comunes son aquellos que forman parte de la de la flora gastrointestinal. La acidez gástrica juega un papel importante en la prevención de la adherencia bacteriana a las paredes del intestino delgado proximal. Sin embargo, ciertas patologías gástricas y duodenales, como son la aclorhidria gástrica patológica o bien, los efectos secundarios por algunos medicamentos, pueden alterar los mecanismos de defensa y favorecer la proliferación bacterina.7,8
La estasis intestinal, causada por obstrucción en la región del yeyuno o íleo, también puede promover la replicación bacteriana. Al realizar cultivos por biopsia transquirúrgica, se ha observado que Echerichia coli está presente en hasta el 56.7% de los casos, seguido de Streptococcus del grupo A en el 25% de los casos y Bacteroides fragilis en el 22.8% de los casos.7,8
Una vez establecido el diagnostico de sepsis, se debe priorizar el inicio de tratamiento, se considera se primera estancia la reanimación hídrica intravenosa con soluciones cristaloides balanceadas, 30 ml/kg, con el propósito de mantener una presión arterial media (PAM) >65 mmHg, y normalizar los niveles de lactato. La monitorización debe ser continua, e incluir presión arterial no invasiva o invasiva según sea el caso, frecuencia cardiaca, saturación de oxígeno medida a través de oximetría de pulso, y cuantificación de diuresis. Algunos otros parámetros de utilidad son la presión venosa central (PVC), en un rango entre 8-12 mmHG, diuresis >0.5 ml/kg/hr, y saturación venosa central de oxígeno (SvcO2) >70%. Debe individualizarse las condiciones de cada paciente y valorar el beneficio de su ingreso a Unidad de Cuidados Intensivos (UCI) cuando sea necesario, para brindad monitorización estrecha y tratamiento oportuno a cualquier eventualidad.5
Lo siguientes criterios se buscan conseguir como meta cuando el tratamiento de un paciente con sepsis se emplea adecuadamente: 1) PAM > 65 mmHg, 2) PVC en rango entre 8-12 mmHg, 3) Diuresis ≥0-5 ml/kg/hora, 4) SvcO2 ≥70%, o bien, una SvO2 > 65%, 5) Lactato sérico < 4 mmol/l y en descenso. Si no se cumplen estos criterios, se deberá replantear el tratamiento, se sugiere repetir la toma de cultivos o considerar la presencia de microorganismos multirresistentes, evaluar si el foco de sepsis requiere de manejo quirúrgico, y por último considerar otra posible etiología como causante de la condición clínica del paciente.7,8
El tratamiento con antibióticos es fundamental y debe iniciarse lo antes posible de manera empírica, inmediatamente después a la toma de cultivos de muestra biológicas relevantes como hemocultivos, urocultivos, cultivos se secreciones o cultivos de colecciones sospechosas de ser el origen de la infección. Estos cultivos ayudaran a identificar el patógeno causante de la infección, y guiar de manera objetiva la antioticoterapia.8
En caso que el manejo conservador con antibióticos no mejore el cuadro clínico, puede ser necesario el tratamiento quirúrgico, sobre todo cuando se sospeche de complicaciones como inestabilidad hemodinámica, o empeoramiento de la misma, o cuando exista aumento en la respuesta inflamatoria sistémica sin causa aparente identificada. La exploración quirúrgica permite evaluar el sitio de la infección, identificar cualquier colección o absceso que pueda estar presente y drenarlo adecuadamente, se pueden realizar procedimientos adicionales, como desbridamiento de tejido infectado, resección de órganos necróticos o reparación de lesiones. Una vez identificado el foco séptico dentro de la cavidad abdominal, debe emplearse el tratamiento quirúrgico tan pronto como sea posible, ya que cualquier retraso mayor a 24 horas aumentara la morbimortalidad significativamente. El abordaje quirúrgico puede realizarse mediante técnicas laparoscópicas, endoscópicas o abiertas, según las indicaciones específicas, en consideración a la experiencia del médico tratante y la disponibilidad de los recursos materiales. El lavado intraperitoneal, el lavado peritoneal continuo en el período postquirúrgico, el desbridamiento radical del peritoneo y el drenaje abdominal por laparotomía han demostrado tener resultados beneficiosos en el manejo de la sepsis abdominal. También se debe considerar la posibilidad de realizar intervenciones percutáneas guiadas por estudios de imagen, como ultrasonido o tomografía axial computarizadas, para el drenaje de abscesos, especialmente en caso de abscesos diverticulares o hepáticas; estos procedimientos percutáneos se combinan con el tratamiento antibiótico adecuado para controlar la infección.8
Ciertos factores se consideran determinantes de mal pronóstico, como edad mayor a 65 años, más de 2 intervenciones quirúrgicas, mal estado nutricional, retraso en el diagnostico e inicio de tratamiento superior a 48 horas, choque séptico asociado a disfunción orgánica múltiple, y falla orgánica múltiple al momento del diagnóstico de sepsis o choque séptico. 9,10
Una herramienta diseñada para la predicción de mortalidad es la escala APACHE (por sus siglas en inglés Acute Physiology and Chronic Health Evaluation), diseñada por primera vez por Knaus a finales de la década de los setentas.11
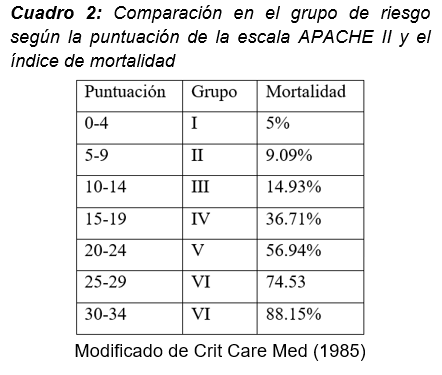
En 1985, se creó una actualización de la ésta escala, renombrada como APACHE II (Cuadro 1), esta escala consta de 12 variables, más una puntuación adicional por edad mayor a 44 años, estado de salud previo del paciente, y la presencia o no de enfermedades crónico-degenerativas. La puntuación de APACHE II se debe calcular al momento del ingreso del paciente y al final del mismo día, de esta manera, nos brinda un perfil momentáneo del estado del paciente. Ésta escala se divide en dos secciones, la primera denominada severidad de la enfermedad en fase aguda o APS (por sus siglas en inglés Acute Physiology Score) que considera variables fisiológicas como la PAM, la frecuencia cardiaca, la frecuencia respiratoria, temperatura, PaO2, pH arterial, y la medición de sodio y potasio séricos, creatinina sérica, hematocrito, leucocitos, más la puntuación en la escala de coma de Glasgow, también se considera en esta sección la medición sérica de bicarbonato (HCO3) cuando se cuente con la PaO2 arterial. A cada una de estas variables le corresponde un puntaje que va de 0 a 4 puntos, la suma de cada puntuación proporcionara el primer componente de la escala APACHE II. La segunda sección, denominada evaluación del estado crónico o CHE (por sus siglas en inglés Chronic Health Evaluation), se refiere al estado de salud previo del paciente; si presenta alguna condición de inmunosupresión, disfunción hepática, cardiaca, renal o respiratoria, o si será sometido a algún procedimiento quirúrgico programado de más de 2 horas de duración, se le sumaran 2 puntos al total ya calculado en la primera sección. En caso de que vaya a ser sometido a algún procedimiento de urgencia, se le sumarán 5 puntos al total. Finalmente, la suma de ambas secciones constituirá el puntaje de la escala APACHE II. El puntaje máximo posible de ésta escala es de 71 puntos, un puntaje igual o mayor a 55 puntos es indicativo de una alta tasa de mortalidad (Cuadro 2).12-15

La disfunción orgánica múltiple (DOM) se define como la presencia de disfunción de múltiples órganos de forma progresiva en un paciente enfermo, se caracteriza por el fallo de varios sistemas de órganos como el cardiovascular, respiratorio, renal, hepático y/o neurológico. La hipoperfusión tisular es el principal factor contribuyente de DOM, cuando la perfusión tisular es inadecuada, los tejidos no reciben suficiente aporte de oxígeno y demás nutrientes, causando el fallo. La saturación venosa mixta de oxígeno (SvO2) y la saturación venosa central de oxígeno (SvcO2) son dos indicadores importantes del estado de oxigenación tisular y el aporte de oxígeno a los tejidos; la SvO2 se refiere a la saturación de oxígeno en la sangre venosa mixta, que es la sangre que retorna al corazón desde los tejidos. Por otra parte, la SvcO2 mide la saturación de oxígeno en la sangre venosa que se extrae directamente de la vena cava superior. Estas mediciones son útiles porque reflejan la cantidad de oxígeno que está siendo entregado a los tejidos (DO2) en relación con la demanda de oxígeno de los tejidos (consumo de oxígeno, VO2). Si la SvO2 o la SvcO2 son bajas, indica que los tejidos no están recibiendo suficiente oxígeno en relación con sus necesidades. El equilibrio entre el aporte de oxígeno (DO2) y el consumo de oxígeno (VO2), es decir la relación DO2/VO2, es fundamental para mantener una adecuada perfusión tisular; si el aporte de oxígeno deficiente para cubrir las necesidades metabólicas de los tejidos, puede ocurrir hipoperfusión tisular y, eventualmente, disfunción orgánica múltiple. Es importante destacar que el monitoreo de la SvO2 y la SvcO2 son herramientas útiles en el cuidado del paciente críticamente enfermo, pero no es el único factor a tener en cuenta, otros parámetros clínicos y de laboratorio, como la presión arterial, el lactato sanguíneo y los niveles de gases en sangre, también son importantes para evaluar la perfusión tisular y el estado de los órganos en un paciente, en manejo integral de la DOM requiere un enfoque multidisciplinario y una intervención clínica adecuada para mantener la homeostasis y mejorar el pronóstico del paciente.16
La medición de la SvO2 se realiza con una muestra extraída directamente desde la arteria pulmonar, a través de catéteres pulmonares, por lo que su obtención es más difícil. En los últimos años, se ha preferido la monitorización de la SvcO2, pues implica un método más simple de obtención, y para la evaluación del aporte global de oxígeno según la situación clínica.16
El contenido venoso mixto de oxígeno (CvO2) es la medición de la cantidad de oxígeno presente en la sangre venosa que retorna al corazón desde los tejidos; cuando el consumo de oxígeno es constante y el contenido arterial de oxígeno (CaO2) se mantiene estable, el CvO2 refleja la relación entre el VO2 y el gasto cardiaco. El VO2 representa la cantidad de oxígeno que los tejidos consumen para llevar a cabo sus funciones metabólicas, el gasto cardiaco, por otro lado, es la cantidad de sangre que el corazón bombea por minuto y está determinado por el volumen sistólico y la frecuencia cardíaca. SvO2 es el principal componente determinante del CvO2, en condiciones fisiológicas normales, el oxígeno disuelto en el plasma sanguíneo es insignificante en comparación con la cantidad de oxígeno transportado por la hemoglobina, por lo tanto, la principal variable que impacta en la SvO2 es la saturación de oxígeno en la hemoglobina. De acuerdo con la ecuación de Fick, el VO2 tisular es proporcional al gasto cardiaco y el CvO2 representa el contenido venoso total del retorno venoso. La SvO2 se mide mediante el análisis de sangre venosa mixta. Es importante destacar que el contenido venoso mixto de oxígeno también puede ser influenciado por otros factores, como la concentración de hemoglobina en la sangre y la afinidad de la hemoglobina al oxígeno, sin embargo, en condiciones fisiológicas estables y durante el período de medición, se considera que estos factores se mantienen constantes, lo que permite establecer una relación entre la SvO2 y el oxígeno contenido a nivel tisular.16,17
La medición de la SvcO2 se realiza típicamente en la aurícula derecha o en la vena cava superior, utilizando un catéter colocado en una de estas ubicaciones, la saturación venosa central refleja el contenido venoso de la parte superior del cuerpo y puede proporcionar información sobre el estado de oxigenación de los tejidos en esa área, sin embargo, es necesario tener en cuenta que la medición de la SvcO2 puede variar según el retorno venoso y la posición de la punta del catéter. La posición y el nivel de SvcO2 pueden cambiar si el catéter se desplaza o si hay cambios en el flujo sanguíneo o en el volumen de sangre que retorna al corazón.18
La SvO2 podría verse disminuida en patologías como hipoxemia, aumento del consumo de oxígeno, disminución del gasto cardiaco y anemia. Un nivel de corte critico de oxígeno medido a través de la SvO2, es aproximadamente un 40%, el cual podría ser más acentuado si el gasto cardiaco no puede adaptarse a los requerimientos metabólicos. A continuación, se enlistan los valores de SvO2 y su representación a nivel de perfusión tisular: 19,20
Las indicaciones para la monitorización de la SvcO2 son sepsis grave y choque séptico, cirugía mayor, insuficiencia cardíaca, trauma grave y choque hemorrágico.19,20
Material y métodos
Se trata de un estudio de concordancia diagnóstica, observacional, comparativo, retrospectivo, en el cual se incluyeron los expedientes clínicos de pacientes con diagnóstico de sepsis abdominal, quienes, sometidos a tratamiento quirúrgico como parte de su manejo, fueron clasificados en la escala APACHE II, y se realizó la determinación de la SvcO2.
El análisis estadístico de la investigación se efectuó utilizando el software R, abarcando métodos descriptivos e inferenciales para una evaluación exhaustiva de las variables relevantes. Este enfoque permitió una interpretación detallada de los datos recolectados.
Se realizó un análisis descriptivo para las variables cuantitativas y categóricas, incluyendo la edad, el sexo, las comorbilidades y los niveles de SvCO2. Se calcularon medidas de tendencia central y dispersión para las variables cuantitativas, y frecuencias y porcentajes para las categóricas.
Para comparar variables cuantitativas entre grupos, se emplearon pruebas estadísticas adecuadas. La prueba t de Student y ANOVA se utilizaron para datos con distribución normal, mientras que para datos no normales se recurrió a pruebas no paramétricas como Mann-Whitney o Kruskal-Wallis.
El análisis de correlación, utilizando el coeficiente de Spearman según la normalidad de los datos, fue crucial para explorar relaciones entre variables cuantitativas como el puntaje APACHE II y los niveles de SvCO2.
Los modelos de regresión logística se utilizaron para identificar factores predictivos de mortalidad, ajustando por posibles variables confusoras. Además, se utilizaron curvas ROC y se calculó el área debajo de la curva ROC (AUC. Se obtuvieron puntos de corte mediante índice J y la significancia estadística se estableció en un valor de p < 0.05 para todas las pruebas.
La muestra total del estudio incluyó a 56 pacientes con diagnóstico de sepsis abdominal, de los cuales 26 (46 %) son femenino y 30 (54 %) masculino. La mediana de edad para la muestra completa fue de 60 años.
En lo que respecta a las comorbilidades prevalentes en la muestra estudiada, la hipertensión arterial (HTA) y la diabetes mellitus tipo 2 (DM2) fueron factores significativos. Se encontró que un 41% de los pacientes (n=23) presentaban hipertensión arterial, mientras que el 59% (n=33) no tenía esta condición. Por otro lado, la diabetes mellitus tipo 2 fue menos común, con solo el 25% (n=14) de los pacientes afectados, en comparación con el 75% (n=42) que no presentaba esta enfermedad crónica.
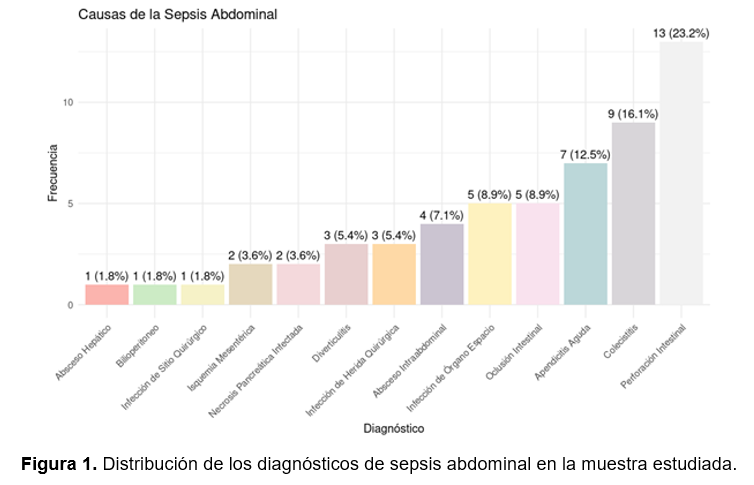
En el análisis de los diagnósticos asociados a la sepsis abdominal, se identificaron trece categorías distintas, siendo la perforación intestinal la más prevalente con 13 casos (23.2%), seguida de colecistitis con 9 casos (16.1%) y apendicitis aguda con 7 casos (12.5%). Los diagnósticos con la menor frecuencia fueron absceso hepático, bilioperitoneo e infección de sitio quirúrgico. Esta diversidad en los diagnósticos refleja el espectro de condiciones que pueden resultar en sepsis abdominal. La Figura 1 ilustra la distribución completa de los diagnósticos en la muestra estudiada.
Además de los diagnósticos variados, se documentaron diversos procedimientos quirúrgicos ejecutados en respuesta a la sepsis abdominal. Predominantemente, la laparotomía exploratoria fue el procedimiento más frecuente, llevado a cabo en 47 de los 56 casos, representando el 83.9% de todos los procedimientos.
Previamente a la realización de los procedimientos quirúrgicos pertinentes en la gestión de la sepsis abdominal, se evaluó la clasificación ASA de los pacientes, que refleja el estado físico preoperatorio y el riesgo anestésico. Se encontró que la mayoría de los pacientes con sepsis abdominal fueron clasificados como ASA III, con un total de 31 pacientes (55.4%), mientras que, 25 pacientes (44.6%) se clasificaron como ASA IV.
La saturación venosa central de oxígeno (SvCO2) es un parámetro clínico importante en la evaluación de la oxigenación y la perfusión tisular en pacientes con sepsis abdominal. En la muestra del estudio, los valores de SvCO2 variaron ampliamente, con un mínimo de 29%, lo que indica una posible perfusión tisular inadecuada, y un máximo de 98%, que podría reflejar una condición hiperdinámica. La mediana fue del 81%, situándose por encima del umbral típico del 70%, lo que sugiere que, en general, la muestra no presentaba un déficit grave de oxigenación. Sin embargo, la variabilidad en los valores de SvCO2 refleja la heterogeneidad en la respuesta fisiológica de los pacientes con sepsis abdominal, lo cual es esencial para la toma de decisiones clínicas.
La distribución de los puntajes APACHE II en pacientes con sepsis abdominal es un indicador crítico de la severidad de la enfermedad y la mortalidad anticipada. En la muestra estudiada, los puntajes APACHE II varían desde un mínimo de 2, que sugiere una menor gravedad, hasta un máximo de 34, lo que indica una condición extremadamente grave. La mediana del puntaje se sitúa en 14, lo cual está ligeramente por encima de la mitad del rango máximo posible de 71 puntos para el puntaje APACHE II, sugiriendo que muchos pacientes presentan un riesgo moderado a alto.
La evaluación de la supervivencia en el contexto del presente estudio revela que, de los 56 pacientes analizados, un total de 14 (25%) no sobrevivieron, mientras que la mayoría, 42 (75%), lograron sobrevivir durante el periodo de estudio. Este dato resalta un significativo porcentaje de supervivencia en la muestra estudiada.
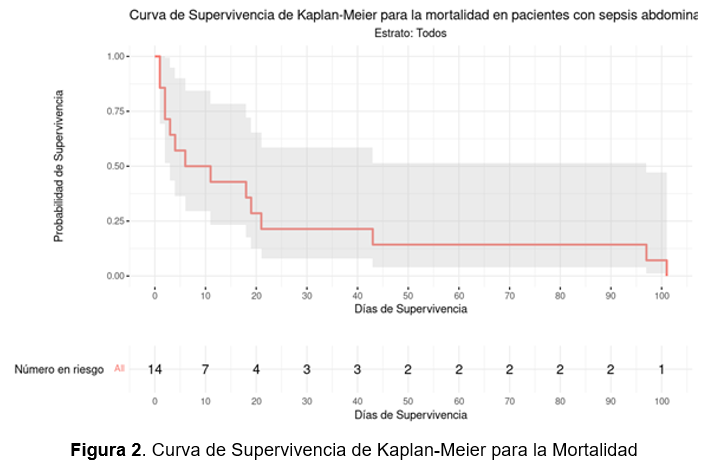
El análisis de la curva de Kaplan-Meier, se muestra que la mediana de supervivencia para el grupo completo es de 8.5 días. Esto significa que el 50% de los pacientes sobrevivió menos de 8.5 días y el otro 50% sobrevivió más tiempo. La curva proporciona también una estimación del intervalo de confianza del 95%, que se extiende desde 3 días como límite inferior hasta 97 días como límite superior, indicando la variabilidad en la supervivencia dentro de la muestra (Figura 2).
El análisis comparativo de los valores de APACHE II y SvCO2 entre los pacientes que sobrevivieron y aquellos que no, revela diferencias estadísticamente significativas, lo que sugiere que estos parámetros podrían tener un papel importante en la determinación de la supervivencia de los pacientes con sepsis abdominal, tal como se muestra en el cuadro 3.
Específicamente, la mediana del puntaje APACHE II fue significativamente más alta en el grupo de no sobrevivientes con una mediana de 17 puntos (rango intercuartílico [IQR]: 15 a 22), en comparación con los sobrevivientes, donde la mediana fue de 10 puntos (IQR: 6 a 17). Este resultado, con un valor de p de 0.002, indica que los pacientes que no sobrevivieron tenían, en promedio, un estado inicial más grave al ingreso.

Por otro lado, la saturación venosa central de oxígeno (SvCO2), presentó diferencias significativas entre los grupos. Los no sobrevivientes mostraron una mediana de SvCO2 considerablemente más baja de 63% (IQR: 56 a 75%), mientras que los sobrevivientes tuvieron una mediana más alta de 85% (IQR: 76 a 90%), con un valor de p de 0.002. Esto sugiere que los pacientes que no sobrevivieron experimentaron una peor oxigenación o un mayor consumo de oxígeno, lo que podría estar relacionado con una mayor gravedad de su estado clínico.
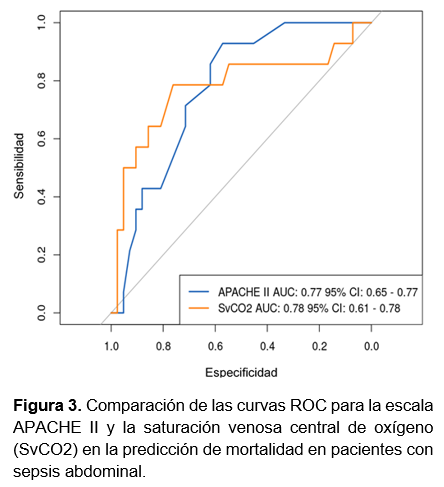
Con el objetivo de hacer un análisis más profundo acerca de la precisión diagnóstica de estos parámetros, la figura 3 muestra las curvas de Características Operativas del Receptor (ROC) para dos predictores de mortalidad en pacientes con sepsis abdominal: la escala APACHE II y la saturación venosa central de oxígeno (SvCO2).
Discusión y resultados
La sepsis abdominal es una condición compleja y multifacética, caracterizada por una respuesta inflamatoria sistémica a una infección intraabdominal. En este estudio, se observó una mediana de edad de 60 años en los pacientes, con una mayor variabilidad en el grupo femenino. Este hallazgo es consistente con la literatura que identifica la edad avanzada como un factor de riesgo significativo en pacientes con sepsis, como se observa en el estudio de Carrillo-Esper et al. (2009)1. Además, la prevalencia de comorbilidades como la hipertensión arterial y la diabetes mellitus tipo 2 en nuestra muestra, que fue del 42% y 26% respectivamente, resalta la importancia de estas condiciones en la sepsis abdominal. Estos datos son consistentes con la investigación de García et al. (2018)2, que identificó estas comorbilidades como factores frecuentes en pacientes con sepsis.
En cuanto a la SvcO2, la mediana del 81% con un rango amplio refleja la variabilidad en la respuesta fisiológica de los pacientes.10
El puntaje APACHE II, con una mediana de 14 en nuestra muestra, sugiere un riesgo moderado a alto en muchos pacientes. Este hallazgo es coherente con estudios como el de Bohnen et al. (1988)15, que también reportaron una correlación entre puntajes APACHE II más altos y peores resultados en sepsis abdominal. Además, un estudio reciente comparó los sistemas de puntuación APACHE II, P-POSSUM y SAPS II en pacientes con peritonitis secundaria sometidos a laparotomías planificadas, encontrando que el APACHE II tenía una alta sensibilidad y especificidad para predecir la mortalidad.21
La tasa de supervivencia del 75% en nuestra muestra, con una mediana de supervivencia de 8.5 días según la curva de Kaplan-Meier, es un dato crucial para entender la progresión de la sepsis abdominal y su impacto en la supervivencia del paciente. Estos resultados son importantes para comparar con estudios como el de Rivers et al. (2001)8, que investigaron terapias dirigidas a objetivos tempranos en el tratamiento de la sepsis severa y el choque séptico, destacando la variabilidad en la supervivencia de estos pacientes.
El análisis predictivo basado en curvas ROC y regresión logística en nuestro estudio proporciona una perspectiva valiosa sobre la capacidad de ciertos parámetros clínicos para predecir la mortalidad. Las curvas ROC para la escala APACHE II y la SvCO2 mostraron un AUC de 0.77 y 0.78, respectivamente, indicando una precisión diagnóstica moderadamente alta. La combinación de APACHE II y SvCO2 en un modelo predictivo mejoró la capacidad de predecir la mortalidad, con un AUC combinado de 0.84. Este enfoque multifactorial es respaldado por la literatura, donde se enfatiza la importancia de considerar múltiples factores en la evaluación del riesgo en pacientes críticamente enfermos.11-15
Es importante reconocer las limitaciones de este estudio. La muestra estudiada, aunque representativa, podría no capturar todas las variaciones y complejidades de la sepsis abdominal en diferentes contextos o poblaciones. Además, la naturaleza retrospectiva de algunos datos puede limitar la interpretación de las tendencias temporales y las relaciones causales. Estas limitaciones subrayan la necesidad de estudios adicionales, preferiblemente multicéntricos y con muestras más grandes, para validar y ampliar nuestros hallazgos.
Los hallazgos de este estudio proporcionan una comprensión integral de la sepsis abdominal, destacando la importancia de una evaluación multidimensional que incluya factores clínicos y demográficos. La identificación temprana de pacientes de alto riesgo mediante parámetros como la SvCO2 y el puntaje APACHE II podría permitir intervenciones más dirigidas y mejorar los resultados clínicos en la sepsis abdominal. Estos hallazgos, junto con las limitaciones del estudio, destacan la necesidad de futuras investigaciones para una comprensión más profunda y un manejo más efectivo de la sepsis abdominal.
Conclusión
El estudio reveló que tanto la SvCO2 como la escala APACHE II son indicadores predictivos significativos de la mortalidad en pacientes con sepsis abdominal. Se observó que los pacientes que no sobrevivieron tendían a tener valores más bajos de SvCO2 y puntajes más altos en la escala APACHE II, lo que refleja una peor oxigenación y una mayor gravedad del estado clínico. Curiosamente, la combinación de estos dos parámetros proporcionó una herramienta de pronóstico más robusta y fiable que cualquiera de los dos por separado, mejorando así la precisión diagnóstica en la predicción de la mortalidad. Estos hallazgos sugieren la importancia de utilizar un enfoque multifactorial en la evaluación y manejo de pacientes con sepsis abdominal, poniendo énfasis en la necesidad de considerar tanto los parámetros clínicos como los demográficos para optimizar las intervenciones y mejorar los resultados clínicos.
Referencias