
Rev Med UAS
Vol. 13: No. 1. Enero-Marzo 2023
ISSN 2007-8013
Karen Analí García-Medina1,2*, Efraín Romo-García1,2
* Correspondencia: Karen Analí García-Medina
Departamento de Retina y vítreo, Hospital Civil de Culiacán/Centro de Investigación y Docencia en Ciencias de la Salud, Culiacán, Sinaloa, México.
Prolongación Álvaro Obregón 1422, Tierra Blanca, 80030 Culiacán Rosales, Sinaloa, México
DOI http://dx.doi.org/10.28960/revmeduas.2007-8013.v13.n1.005
Texto Completo PDFRecibido 2 de marzo 2023, aceptado 29 de abril 2023
RESUMEN
Objetivo: determinar la concordancia en el diagnóstico y clasificación de la retinopatía diabética utilizando imágenes de fondo de ojo de campo ultra amplio, comparando los sistemas Optos® y Clarus 700®. Materiales y métodos: se realizó un estudio comparativo, descriptivo, prospectivo y transversal en el que se incluyeron 144 ojos de 77 pacientes (41 hombres y 36 mujeres) para con una confianza del 95%, estimar el coeficiente de concordancia K (kappa). --- Resultados: el coeficiente Kappa de Cohen obtenido fue de .846, que se traduce como una concordancia muy buena entre los sistemas Optos® y Clarus 700® en el diagnóstico y clasificación de la retinopatía diabética utilizando imágenes de fondo de ojo de campo ultra amplio. --- Conclusiones: ambos sistemas de imagen de fondo de ojo de campo ultra-amplio mostraron ser similares en el diagnóstico y clasificación de la retinopatía diabética; sin embargo, Optos® permitió imágenes de fondo de ojo más amplias que Clarus 700®; mientras que Clarus 700® produjo menos artefactos y proporcionó imágenes más detalladas del fondo de ojo. No se tiene registro de estudios previos que comparen ambos sistemas de campo ultra amplio que se hayan realizado en México, lo cual permite utilizar la información obtenida como base para estudios posteriores.
Palabras clave. Diabetes mellitus, retinopatía diabética, sistemas de imágenes retinales de campo ultra amplio.
ABSTRACT
Objective: to determine the concordance in the diagnosis and classification of diabetic retinopathy using ultra-wide field fundus images, comparing the Optos® and Clarus 700® systems. --- Materials and methods: a comparative, descriptive, prospective and cross-sectional study was carried out in which 144 eyes of 77 patients (41 men and 36 women) were included to estimate the K (kappa) concordance coefficient with a confidence of 95%. --- Results: Cohen's Kappa coefficient obtained was .846, which translates as very good agreement between the Optos® and Clarus 700® systems in the diagnosis and classification of diabetic retinopathy using ultra-wide field fundus images. --- Conclusions: both ultra-wide field fundus imaging systems proved to be similar in the diagnosis and classification of diabetic retinopathy; however, Optos® allowed for larger fundus images than Clarus 700®; while Clarus 700® produced fewer artifacts and provided more detailed fundus images. There is no record of previous studies that compare both ultra-wide field systems that have been carried out in Mexico, which allows using the information obtained as a basis for subsequent studies.
Keywords. Diabetic mellitus, diabetic retinopathy, Ultra-wide-field retinal imaging systems.
INTRODUCCIÓN
La vista es uno de los sentidos más importantes del ser humano debido a que le permite ser independiente y realizar sus actividades día a día. La visión es percibida gracias a una extensión de neuronas que forman un complejo llamado retina, el cual presenta demandas metabólicas excepcionalmente altas; por lo que cuenta con dos lechos vasculares que la nutren, cada uno de los cuales con una anatomía y fisiología distintas.
La retina externa se encuentra irrigada por la capa coriocapilar, mientras que la retina interna se nutre a través de la vasculatura intrarretiniana.1
Existen múltiples enfermedades sistémicas que pueden afectar la visión, una de las más importantes es la Diabetes mellitus (DM) causante de la retinopatía diabética (RD), enfermedad que puede conducir a la ceguera.
Los avances en las imágenes de la retina y el análisis funcional de la misma, indican que antes del desarrollo de la RD clínicamente identificable, existen patologías vasculares y neurales que la preceden. El diagnóstico precoz de estas alteraciones podría facilitar el tratamiento oportuno en pacientes de alto riesgo; los antagonistas de la vía del factor de crecimiento endotelial vascular disminuyen con suma eficacia la pérdida de la visión y promueven una mejoría clínica importante en pacientes atendidos de manera temprana.2
Se han observado cambios transcripcionales en la microglía activada, mediados a través del factor kappa de cadena ligera que actúa como potenciador de células B activadas (NFκB) y regulado por señales extracelulares, lo que da como resultado la liberación de diversos mediadores proinflamatorios.
Una de las consecuencias más importantes de estos cambios en la microglía, es la afectación grave de las neuronas de la retina, que provoca un aumento de la apoptosis y el consiguiente adelgazamiento de la capa de fibras nerviosas que se traduce en pérdida visual en el paciente.3
Se considera que la retinopatía es la complicación más común de la diabetes y una de las causas más importantes de ceguera en pacientes en edad laboral a nivel mundial.
Después de la declaración de San Vicente de reducir la ceguera por Diabetes mellitus en un tercio, el Reino Unido se convirtió en el primer país en el mundo en ofrecer proyecciones organizadas sistemáticamente para la RD a todos los pacientes mayores de 12 años de edad diagnosticados con la enfermedad.
El cribado es supervisado por el Programa Nacional de Cribado Ocular para Diabéticos; en este programa, se realiza la toma de fotografías de la retina bajo midriasis farmacológica, posteriormente un calificador especializado valora las imágenes y los resultados de las mismas. De ser necesario, se envía a los pacientes a servicios hospitalarios para tratamiento o se derivan a medicina general según sea el caso, de no detectar retinopatía, se le indica al paciente la importancia de una revisión anual.4
En la última década se ha descrito que existen diversos factores que contribuyen con los cambiantes patrones de epidemiología de la RD, tales como: carga genética para la enfermedad, avances en el diagnóstico y tratamiento y acceso a los servicios de salud.5
Se ha establecido que la Diabetes mellitus aumenta el riesgo de enfermedad cardiovascular. Cheng et al., encontró que la prevalencia de RD asociada con uno, dos, tres o cuatro factores de riesgo cardiometabólico es de 16%, 17.6%, 21% y 25.1%, respectivamente; lo cual implica una relación entre las condiciones de salud sistémicas y la retinopatía diabética.6
Está descrito que se pueden detectar anomalías en la función de la retina en pacientes sin evidencia de anomalías microvasculares; por su parte, la Asociación Estadounidense de Diabetes, recientemente definió a la RD como una complicación neurovascular altamente específica.7
A nivel mundial, China tiene el mayor número de personas afectadas por Diabetes mellitus, lo cual representa una carga enorme para el sistema de salud; ya que como se ha mencionado anteriormente, la Diabetes puede ocasionar enfermedades en diferentes órganos del cuerpo, principalmente: corazón, cerebro, riñón, sistema nervioso y retina; así como la afectación de las extremidades lo cual representa un daño importante a la población laboralmente activa.8
En países como la India, existen dos modelos de cribado, los cuales se basan en modelos oftalmológicos; estos implican la detección por un médico oftalmólogo que utiliza la oftalmoscopía indirecta de manera aislada o en conjunto con fotografías de fondo de ojo para valorar la retina. El otro modelo que se practica es el modelo de teleprotección en el cual participa personal paramédico quien realiza la toma de imágenes las cuales son evaluadas por médicos oftalmólogos certificados quienes otorgan una calificación de manera remota a las mismas.9
Se han desarrollado tres mecanismos estratégicos para prevenir la ceguera causada por la retinopatía diabética: el primer mecanismo es la prevención primaria y consiste en prevenir o retrasar la aparición de la retinopatía en personas diabéticas; el segundo: la prevención secundaria, tiene la finalidad de evitar la progresión de la RD en pacientes con retinopatía establecida; por último, la prevención terciaria, se enfoca en prevenir la ceguera por retinopatía diabética.10
Hace poco más de medio siglo, el 29 de septiembre de 1968, un consorcio internacional de líderes en oftalmología, medicina y neurocirugía se reunieron en la Airlie House, Warrenton, para abordar el creciente problema de salud que representaba la retinopatía diabética como una de las principales causas de ceguera.11
En la actualidad, con el apoyo de técnicas de imagen más avanzadas, como la Tomografía de Coherencia Óptica (OCT), OCT con angiografía e imágenes de campo ultra amplio (imágenes de hasta 200° de la retina en una sola toma), se demostró que existen otros elementos que participan en la aparición de la retinopatía y el edema macular diabético, incluida la inflamación y la neurodegeneración.12
Una causa importante de pérdida visual en pacientes con RD es el edema macular, que se caracteriza por aumento del grosor macular debido a la acumulación de líquido intrarretiniano ocasionado por la ruptura de la barrera hematorretiniana; éste puede presentarse en cualquier etapa de la enfermedad y ocasionar distorsión de las imágenes visuales y disminución de la agudeza visual.13
Diversos estudios han indicado que en un número importante de pacientes con DM no se indicó un examen oftalmológico anual debido al largo tiempo de espera para las valoraciones, la asintomatología de los pacientes y un acceso limitado a especialistas en retina.14
El advenimiento de imágenes de campo ultra amplio (UWF), ha permitido la visualización de la retina periférica lejana; áreas que están más allá del campo de imagen de fotografías tradicionales de 7 campos. Ejemplo de equipos capaces de obtener imágenes de UWF son: Optos California® [Optos PLC, Dunfermline, Reino Unido] y Clarus 700® [Carl Zeiss Meditec, Jena, Alemania].15
Las imágenes de UWF representan un avance importante en la detección y el manejo de la retinopatía diabética. Los datos actuales sugieren que las imágenes de UWF, en comparación con los campos convencionales del Estudio para el Tratamiento Temprano de la Retinopatía Diabética (ETDRS), detectan patologías de retinopatía diabética proliferativa (RDP) adicionales y más extensas, y al permitir visualizar una mayor extensión de retina en pacientes con retinopatía diabética no proliferativa (RDNP), agregan un valor pronóstico en términos de progresión hacia la variedad proliferativa.16
El uso de imágenes que permiten valorar de manera mucho más precisa la periferia de la retina ha permitido ofrecer un mejor diagnóstico y tratamiento a pacientes con alteraciones especialmente sensibles en estas zonas periféricas del fondo de ojo. Las imágenes de campo ultra amplio pueden no ser clínicamente necesarias para todas los pacientes, sin embargo, son una herramienta importante en pacientes de alto riesgo.17
En la actualidad, el estándar de oro para la valoración de fondo de ojo es el del ETDRS; si bien la visualización de los siete campos que se valoran cubre la mayoría de la retina central; muestra solo aproximadamente el 30% de toda la superficie retiniana. Por lo anterior es que han surgido nuevos métodos que reducen el tiempo y los recursos invertidos para la detección de la enfermedad; por ejemplo, el láser oftalmoscópico de escaneo Optos®.
El sistema Optos® utiliza un campo ultra amplio y puede proporcionar 200° de visión de la superficie de la retina en una sola imagen, comparado con el método convencional que requiere de hasta 16 imágenes para igualarlo.18
En un intento por solucionar la escasez de médicos especialistas en oftalmología se realizó un estudio en el que cinco médicos de medicina familiar recibieron una conferencia de una hora sobre la RD por parte de un especialista en retina, posteriormente, a los médicos se les mostraron 30 imágenes de retina de campo ultra amplio y se les pidió que determinaran si las imágenes presentaban signos de retinopatía diabética; los médicos pudieron identificar con precisión las imágenes posteriores a la toma, pero no fueron tan precisos al evaluar imágenes tomadas en la clínica de medicina familiar; de aquí la importancia de mejorar la capacitación del personal para obtener mejores resultados y optimizar los recursos.19
Estudios recientes han demostrado que la angliografía con fluoresceína de campo ultra amplio tiene el potencial de revolucionar la retinopatía diabética en múltiples aspectos; sin embargo, se requieren más ensayos de alta calidad para confirmar las investigaciones previas y traducirlos en la práctica clínica diaria.20
Takahashi et al., utilizaron fotografías de 45° de fondo de ojo, de cuatro campos para capturar un área amplia de la retina para la estadificación de la RD basándose en un algoritmo especial. En el estudio, el uso de imágenes de fondo de ojo de cuatro campos mostró mejores resultados en cuanto a la clasificación de la RD en comparación con una sola imagen de fondo de ojo; sin embargo, la obtención de las imágenes de cuatro campos puede requerir gran cantidad de tiempo y esfuerzo.21
Un sistema de detección de RD debe contar con la capacidad de detectar amenaza a la visión ya sea por la misma retinopatía o por enfermedades como el glaucoma y la degeneración macular relacionada a la edad.
En el campo de la oftalmología, se demostró que las herramientas que involucran el uso de inteligencia artificial, muestran un rendimiento diagnóstico clínicamente aceptable cuando se utilizan fotografías a color del fondo de ojo de la retina, por lo tanto, se considera que los modelos de inteligencia artificial son una solución prometedora en el tema del cribado de la retinopatía diabética.22
En un estudio observacional y prospectivo, se examinaron 50 ojos de 28 pacientes con RD. Un total de 46 ojos de 27 pacientes (19 hombres y 8 mujeres) fueron incluidos en el análisis. En el estudio mencionado previamente, se obtuvo una sola imagen utilizando dos sistemas de imágenes de campo ultra amplio (UWF): Optos® (Optos Carfornia®, Optos PLC, Dunfermline, United Kingdom) y Clarus® (CLARUS 500 ™, Carl Zeiss Meditec Inc., California, EE. UU.), sin midriasis farmacológica. El área total de retina capturada y el área retiniana oscurecida se compararon entre los dos sistemas. El ETDRS y la Escala Internacional de Severidad de la Retinopatía Diabética fueron analizados mediante gráficas estadísticas.
Los resultados obtenidos fueron que el sistema Optos® permitió la captura de áreas más grandes del fondo de ojo en comparación con el Clarus® (465 ± 117 vs.243 ± 39 áreas de disco, P <0,0001). La severidad fue mayor en cuatro imágenes de Clarus® y en una sola imagen Optos®; esto en cinco ojos en los que la Escala Internacional de Severidad de la Retinopatía Diabética difería entre ambos sistemas.
En el estudio previamente mencionado; se concluye que los sistemas de imágenes retinianas de campo ultra amplio, Optos® y Clarus® fueron útiles para examinar ojos con RD, utilizando imágenes individuales obtenidas sin midriasis. Ambos sistemas fueron generalmente consistentes en la evaluación de la gravedad de la enfermedad, con algunas discrepancias parciales; sin embargo, se requiere de más estudios que complementen la información obtenida.23
El presente estudio pretende determinar cuál es la concordancia en el diagnóstico y clasificación de la retinopatía diabética al utilizar imágenes de fondo de ojo de campo ultra amplio obtenidas con el sistema Optos® respecto a las obtenidas en Clarus 700®.
MATERIALES Y MÉTODOS
Se trata de un estudio comparativo, descriptivo, prospectivo y transversal en el que se realizó la toma de imágenes de fondo de ojo de campo ultra amplio con los sistemas Optos® y Clarus 700®; una sola imagen de cada ojo y con ambos equipos fue obtenida (sin midriasis farmacológica inducida) en pacientes con diagnóstico de Diabetes mellitus que acudieron al departamento de Oftalmología del Hospital Civil de Culiacán, se excluyeron a pacientes con tratamiento oftalmológico previo por retinopatía diabética en cualquiera de sus modalidades y se eliminó a quienes no fue posible la toma de imágenes para la valoración de fondo de ojo (opacidad de medios, etc.).
Los criterios de inclusión fueron: ambos géneros, edades de 18 a 80 años, con diagnóstico de Diabetes mellitus sin tratamiento previo para retinopatía diabética y firma del consentimiento informado. Como criterio de exclusión: pacientes con tratamiento previo para retinopatía diabética en cualquiera de sus modalidades; y criterios de eliminación: pacientes en quienes no haya sido posible la toma de las imágenes de fondo de ojo.
Una vez captados los pacientes que cumplieron con los criterios de inclusión, se procedió a la firma del consentimiento informado por el paciente y posteriormente al llenado de la hoja de recolección de datos realizada para el estudio.
Posteriormente se realizó la captura de imagen de fondo de ojo con los sistemas Optos® (Optos California®, Optos PLC, Dunfermline, United Kingdom) y Clarus™ (Clarus 700®, Carl Zeiss
Meditec Inc., California, EE. UU.), sin midriasis farmacológica inducida.
Definición de las variables
Se definió a la retinopatía diabética como una complicación neurovascular altamente específica que afecta las estructuras retinianas; los hallazgos en las imágenes de fondo de ojo se definieron de acuerdo a la Escala Clínica Internacional de Gravedad de la Retinopatía Diabética (figura 1).

Muestra: se estudió una muestra de 144 ojos para con una confianza del 95%, estimar el coeficiente de concordancia K (kappa); suponiendo una concordancia muy buena (0.810) y un porcentaje de positivos del 52% y 48%, para Optos y Clarus 700®, respectivamente.
Recolección de datos: los datos se recolectaron por fuente primaria a través de la anamnesis clínica en la consulta médica.
Análisis estadístico: una vez recolectada la información se procedió al vaciamiento de la misma en una base de datos del paquete informático SPSS (SPSS, Inc., Chicago IL, USA) para su organización, codificación y análisis estadístico; así mismo, se determinó el Coeficiente de concordancia Kappa de Cohen (K) entre ambos sistemas. Los datos fueron presentados en cuadros y figuras.
RESULTADOS
Se incluyeron 144 ojos de 77 pacientes con diagnóstico de Diabetes mellitus, sin antecedente de tratamiento previo por retinopatía diabética en ninguna de sus modalidades.
De los 77 pacientes que participaron en el estudio, 41 fueron hombres y 36 mujeres; representando el 53.2% y 46.8% del total de los participantes, respectivamente (cuadro 1); con edades entre 18 y 85 años (cuadro 2).


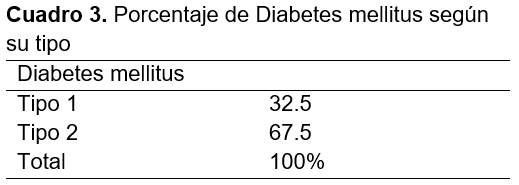
El tipo de Diabetes mellitus más frecuente fue el tipo 2, presente en 52 pacientes, mientras que el tipo 1 se encontró en 25 de los participantes; representando un 67.5% y 32.5%, respectivamente (cuadro 3).
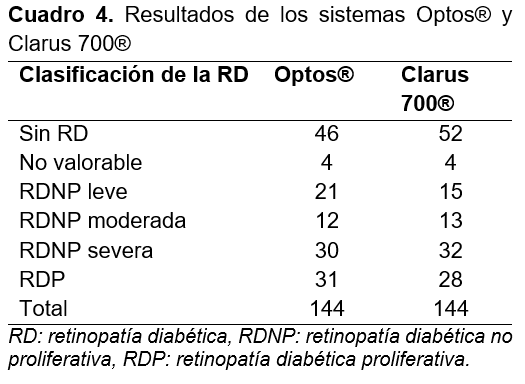
Los resultados del sistema Optos® fueron los siguientes: sin retinopatía: 46 ojos, no valorable por opacidad de medios (catarata) 4, RDNP leve 21, RDNP moderada 12, RDNP severa 30 y RDP 31. Mientras que en el sistema Clarus 700® se observaron 52 ojos sin retinopatía, 4 no valorables por opacidad de medios (catarata), 15 con RDNP leve, 13 RDNP moderada, 32 RDNP severa y 28 con RDP (cuadro 4).
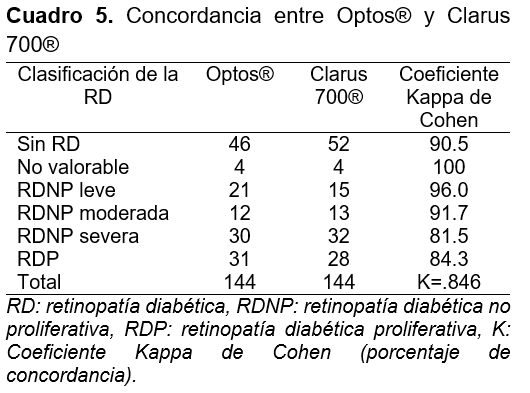
De acuerdo a los resultados; se obtuvo una concordancia entre los equipos Optos® y Clarus 700® en: 90.5% de los pacientes sin evidencia de retinopatía diabética, 100% en los pacientes en quienes no fue posible realizar una valoración por opacidad de medios (catarata), 96.0% en RDNP leve, 91.7% RDNP moderada, 81.5% RDNP severa y 84.3% en retinopatía diabética proliferativa (cuadro 5).
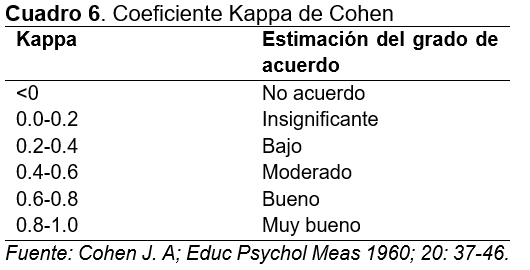
El coeficiente Kappa de Cohen fue de .846, que se traduce como una concordancia muy buena entre los sistemas Optos® y Clarus 700® en el diagnóstico y clasificación de la retinopatía diabética utilizando imágenes de fondo de ojo de campo ultra amplio (Cuadro 6).
DISCUSIÓN
La presente investigación realizó la comparación de la concordancia entre dos sistemas de imagen retiniana de campo ultra amplio, los equipos Optos® y Clarus 700®. El estudio consistió en valorar ojos de pacientes con diagnóstico de Diabetes mellitus, utilizando imágenes únicas obtenidas sin midriasis farmacológica inducida, en ninguno de los casos.
El sistema Optos® permitió la captura de áreas más grandes del fondo de ojo en comparación con el sistema Clarus 700®. Un dato interesante es que artefactos presentes en las imágenes de Optos®, como las pestañas, dificultan, aunque no en todos los casos, la valoración de zonas periféricas de la retina superior e inferior, lo cual no ocurre con las imágenes de Clarus 700® ya que el equipo es capaz de reducir los artefactos en los párpados y las pestañas, probablemente debido a la óptica parcialmente confocal incluida en el sistema.
La concordancia entre los equipos Optos® y Clarus 700® en la Escala Clínica Internacional de Gravedad de la Retinopatía Diabética fue muy buena, con un coeficiente Kappa de Cohen de .846; lo que indica que ambos equipos son útiles en el diagnóstico y clasificación de la retinopatía diabética.
En general, la gravedad de la retinopatía diabética fue mayor en el sistema Optos® en comparación con Clarus 700®; aun cuando en algunos ojos, áreas de la retina no pudieron ser examinadas en las imágenes de Optos® debido a la presencia de artefactos.
Sin embargo, en otros casos, Clarus 700® presentó discrepancias debido a que permite la valoración de áreas retinianas inferiores en donde fue posible identificar restos de hemorragia vítrea antigua lo cual cambia por completo la clasificación de la retinopatía diabética.
La gravedad fue mayor en seis imágenes en Optos® en los que se determinó RDNP leve mientras que Clarus 700® mostró sin evidencia de retinopatía diabética. Por su parte, el sistema Clarus 700® determinó mayor grado de severidad en retinopatía diabética no proliferativa moderada y severa en ojos con microaneurismas y/o microhemorragias retinianas que solo podía detectarse en imágenes con Clarus 700® debido a que el sistema muestra imágenes con colores reales, ya que como se describe previamente, el efecto de los artefactos se puede mitigar usando la funcionalidad y las instancias de la óptica parcialmente confocal permitiendo representar imágenes en color verdadero.
De acuerdo a la hipótesis, la gravedad fue mayor en las imágenes de Optos® debido a que permite capturar mayor área retiniana en comparación con el sistema Clarus 700®.
Como tal, al realizar evaluaciones que requieren imágenes individuales obtenidas sin midriasis, el sistema Clarus 700® puede ser más adecuado que el sistema Optos® respecto a la claridad y representación real de las imágenes; sin embargo, se ha sugerido que el sistema Optos® puede identificar anomalías retinianas periféricas iniciales en pacientes con retinopatía diabética.
Por ejemplo, los pacientes que presentaron mayor grado de severidad en la Escala Clínica Internacional de Gravedad de la Retinopatía Diabética, fueron en su mayoría, aquellos con hemorragias retinianas periférica que no se detectaron con el equipo Clarus 700®.
Se considera que ambos equipos utilizados en este estudio cuentan con mucho más potencial, es decir; adquirimos solo imágenes individuales sin midriasis ya que es una característica de los sistemas, sin embargo, imágenes midriáticas tomadas con el sistema Optos® son, según se informa, de mejor calidad que las imágenes no midriáticas.
Combinando las imágenes de Optos® de diferentes partes de la retina, es posible la captura de un campo retiniano más amplio, incluso hasta obtener imágenes panretinales. Además, el escaneo en color separado del equipo Optos® potencialmente proporciona información adicional, ya que el escaneo en color verde, "libre de rojo" puede incluir información más selectiva sobre las capas superficiales de la retina neurosensorial.
Por su parte, el sistema Clarus 700® puede combinar imágenes de diferentes regiones de la retina y de esta forma mostrar áreas más grandes del fondo de ojo.
Aunque las imágenes de Optos® fueron menos útiles que las imágenes de Clarus 700® para identificar microaneurismas y/o microhemorragias retinianas, el primero permitió la evaluación de áreas más grandes de la retina.
CONCLUSIÓN
El sistema Optos® puede ser más adecuado que el sistema Clarus 700® para evaluaciones que requieren imágenes de la retina más amplias. Optos® permitió imágenes de fondo de ojo más extensas que Clarus 700®; sin embargo, éste último produjo menos artefactos y proporcionó imágenes más detalladas del fondo de ojo.
Los sistemas de imágenes retinianas Optos® y Clarus 700® son útiles para examinar ojos con retinopatía diabética, utilizando imágenes únicas obtenidas sin midriasis. Ambos equipos fueron generalmente consistentes en la evaluación de la gravedad de la retinopatía, con algunas discrepancias.
No se tiene registro de estudios previos que comparen ambos sistemas de campo ultra amplio que se hayan realizado en México, lo cual permite utilizar la información obtenida como base para estudios posteriores.
Referencias