Rev Med UAS
Vol. 11: No. 2. Abril-Junio 2021
ISSN 2007-8013
Adriana Sarahi Valdez-Radke1, Ruth Acuña-Maldonado2, Carolina Cardona-Estrada3, Efraín Romo-García4.
*Autor de correspondencia: Sarahi Valdez-Radke
adriana_radke@hotmail.com
DOI http://dx.doi.org/10.28960/revmeduas.2007-8013.v11.n2.004
Texto Completo PDFRecibido 28 de Enero 2021, aceptado 12 de Febrero 2021
RESUMEN
Objetivo: Demostrar la disminución de la progresión de miopía en pacientes pediátricos de 5 a 14 años de edad con el uso de atropina al 0.01 %. --- Material y métodos: Se reclutaron un total de 28 pacientes entre 5-14 años de edad, con miopía de ≥-1,50 D y astigmatismo ≥0.50, se les aplicó una dilución de 0.01% de atropina durante un año, se preparaba de manera individualizada y se realizaba un estudio de refracción bajo cicloplejia cada 4 meses. --- Resultados: Se tomaron en cuenta 4 mediciones, al inicio del tratamiento, a los 4, 8, 12 meses de seguimiento, encontrándose una refracción inicial de -4.38±0.56 D, -4.69±0.25 D, -4.64±0.30 y -4.95 respectivamente. Lo que resultó con tendencia estadísticamente significativo (p= 0.05). --- Conclusiones: Se demostró una reducción de la progresión de la miopía de -0.58 D en la población estudiada con atropina al 0,01% durante un año.
Palabras clave: Atropina, Miopía, Progresión, Niños, Dilución.
ABSTRACT
Objective: To demonstrate the decrease in the progression of myopia in pediatric patients 5 to 14 years of age with the use of 0.01% atropine. --- Material and methods: A total of 28 patients were recruited between 5-14 years of age, with myopia ≥-1.50 D and astigmatism ≥0.50, a dilution of atropine 0.01% was applied for one year, it was prepared individually and a refraction study was performed under cycloplegia every 4 months. --- Results: 4 measurements were taken into account, at the beginning of the treatment, at 4, 8, 12 months of follow-up, finding an initial refraction of -4.38 ± 0.56 D, -4.69 ± 0.25 D, -4.64 ± 0.30 and -4.95 respectively resulted with a statistically significant trend (p = 0.05). --- Conclusions: A reduction in the progression of myopia of -0.58 D was demonstrated in the population studied with 0.01% atropine for one year.
Keywords: Atropine, Myopia, Progression, Children, Dilution
INTRODUCCIÓN
La miopía es la anomalía refractiva del ojo en la que el foco visual de la retina está en algún punto finito delante del ojo, cuando el ojo no está acomodando. Se estandariza un equivalente esférico de -5,00 D o menos para la miopía alta porque identifica a las personas con mayor riesgo de miopía patológica y si no se corrigen, causa deterioro de la visión equivalente a la ceguera definida por la Organización Mundial de la Salud.1
En 2010 se estimó que el error refractivo no corregido fue la causa más común de deterioro de la visión a distancia, afectando a 108 millones de personas y la segunda causa más común de ceguera a nivel mundial.2
Se han propuesto diferentes opciones terapéuticas para el tratamiento de la miopía, como son el uso de diferentes tipos de lentes como son los lentes monofocales, bifocales, multifocales, lentes de contacto, la ortokeratologia, cirugía refractiva, así como medicamentos tópicos oftálmicos, por ejemplo, agentes muscarínicos e hipotensores oculares, sin embargo, ninguno de ellos ha probado ser eficaz para la disminución de la progresión de la miopía. Se han propuesto diferentes diluciones de atropina para demostrar la eficacia y seguridad para la progresión de la miopía en niños pediátricos. Inicialmente se propuso atropina 1%, demostrando su efecto benéfico sobre la progresión de la miopía.3. Se propusieron diferentes diluciones con fin de evaluar la eficacia y seguridad de atropina, al 0.5%, 0.01% y 0.01% 4 ,5 otro estudio evalúa concentraciones de atropina al 0.025%, 0.01% y 0.5% 6 demostrando su eficacia y seguridad en la progresión de la miopía en niños.
En este estudio se incluyeron a 28 pacientes del Hospital Civil de Culiacán, de 5 a 16 años, con una edad promedio de 10.21 años, los cuales recibieron una dilución de atropina al 0.01% durante un año como tratamiento para la progresión de la miopía.
MATERIAL Y METODOS
Se trata de un estudio experimental, comparativo, prospectivo, longitudinal, no controlado, no aleatorizado, no ciego.
Se reclutaron pacientes pediátricos con diagnóstico de miopía de 5-14 años que acudan a la consulta de oftalmología pediátrica, con un total de 28 pacientes.
Se realizó en el Hospital Civil de Culiacán en el Área de Oftalmopediatría, en el periodo de tiempo de realización (Fecha de inicio y final) Noviembre 2017-Noviembre 2018
Los criterios de inclusión: Pacientes con miopía de ≥-1,50 D con astigmatismo ≥0.50, sexo indistinto: Masculino/Femenino, paciente con progresión de miopía > - 0.50 en el último semestre o desde la última consulta. Edad: mayor de 5 años y menor de 14 años y que no tuvieran patología a nivel de cualquiera estructura ocular (alteraciones retinianas, catarata, glaucoma) ni patologías sistémicas asociadas.
Los criterios de exclusión: pacientes con miopía de <1,50 D de edad: menores de 4 años y mayores de 15 años, patología ocular (alteraciones retinianas, catarata, glaucoma) y pacientes con diagnóstico de cualquier patología sistémica que condicione o no cualquier error refractivo.
Los criterios de eliminación: pacientes en los que se recaben de forma incompleta las variables estudiadas.
Los datos fueron analizados mediante el análisis de las medias de las mediciones. Para los datos demográficos y datos de efectos adversos se utilizó la prueba exacta de Fisher. Para las variables cuantitativas se utilizó un modelo lineal de ANOVA de medias repetitivas para seguir la tendencia de los datos y conocer si existió un modelo de progresión al efecto del uso de fármaco, se hizo un análisis Posthoc de Bonferroni para comparar los diferentes grupos posterior al análisis de ANOVA, los datos fueron analizados con el software estadístico IBM® SPSS V.22
RESULTADOS
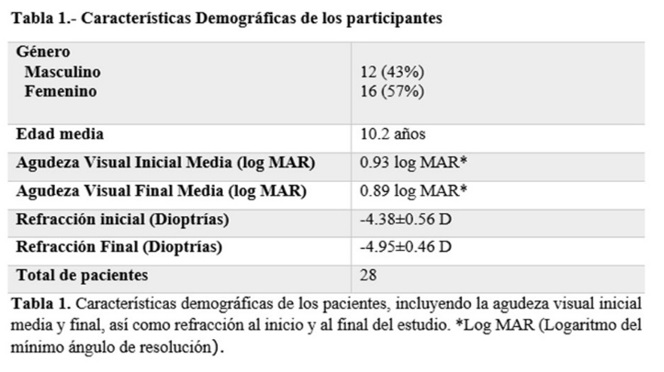
En el presente estudio se analizaron 56 ojos de 28 pacientes del Hospital Civil de Culiacán. Se incluyeron 16 mujeres (57%) y 12 hombres (43%) dentro del grupo de estudio, de 5 a 14 años de edad con una media de 10.2 años. Tabla 1.

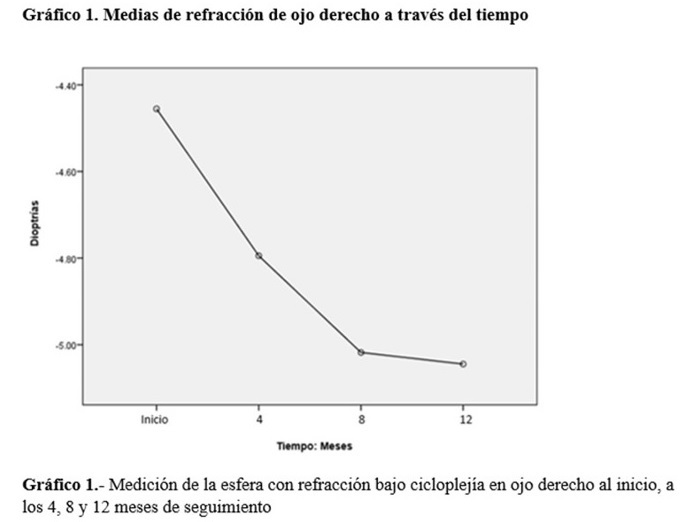
Se realizó un análisis por cada uno de los ojos al inicio, a los 4, 8 y 12 meses de seguimiento, obteniendo los siguientes resultados: en el ojo derecho se encontró una refracción media inicial de -4.75±0.58D (p=0.001), -4.79±0.25D (p=0.085), -5.01±0.02D (p=1.00), -5.04±0.58 (p=0.001), a los 4, 8 y 12 meses respectivamente, resultando estadísticamente significativo durante las 4 mediciones consecutivas que se realizaron, obteniéndose así, una disminución de la progresión de la miopía de -0.59 D por año en el ojo derecho. (Grafico 1).
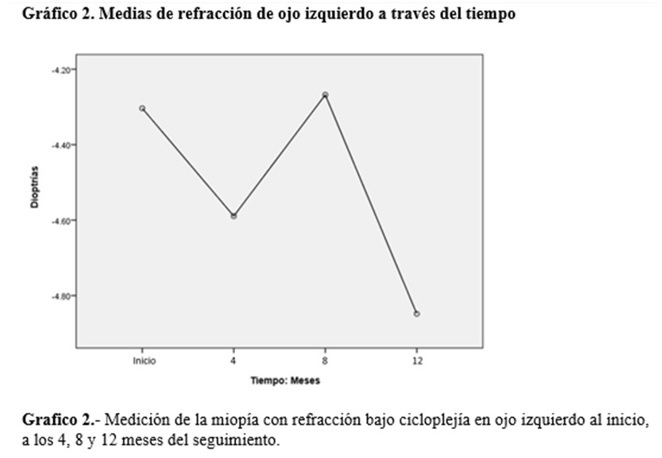
Analizando el ojo izquierdo, se encontró una refracción inicial de -4.30 D±0.54D(p=0.005), -4.58±0,25D (p=0.187), -4.26±0.58D(p=1.00), -4.84±-0.54(p=0.005). (Grafico 2).
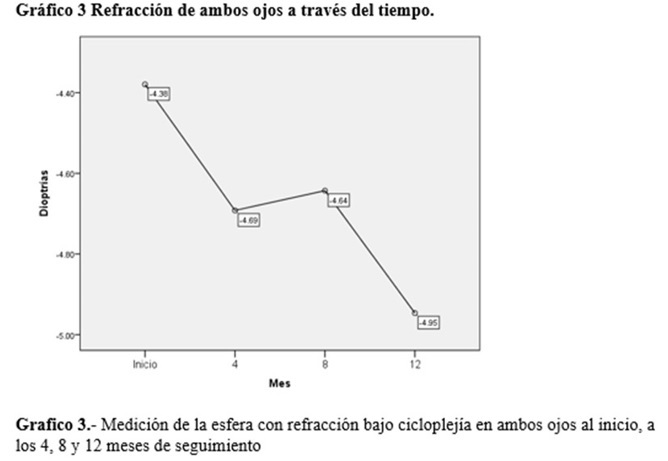
Respecto a la refracción global, es decir el análisis de los 56 ojos, se tomaron en cuenta 4 mediciones, al inicio del tratamiento, a los 4, 8, 12 meses de seguimiento, encontrándose una refracción inicial de -4.38±0.56 D, -4.69±0.25 D, -4.64 ± 0.58) y -4.95±-0.54D respectivamente. Lo que resultó con tendencia estadísticamente significativo p= 0.05. (Gráfico 3).
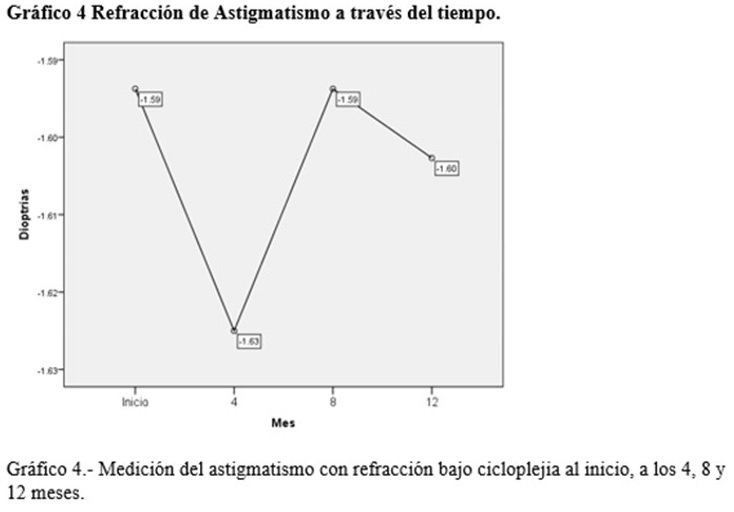
Se realizó el análisis de la progresión del astigmatismo a través del tiempo, se realizaron las mediciones al inicio -1.59±1.08, a los 4, 8 y 12 meses, -1.63±1.13D, -1.59 ±1.10D, -1.60±1.07D, teniendo una diferencia entre la primera medición y la última de -0.001 D, con una p=0.975. (Gráfico 4).
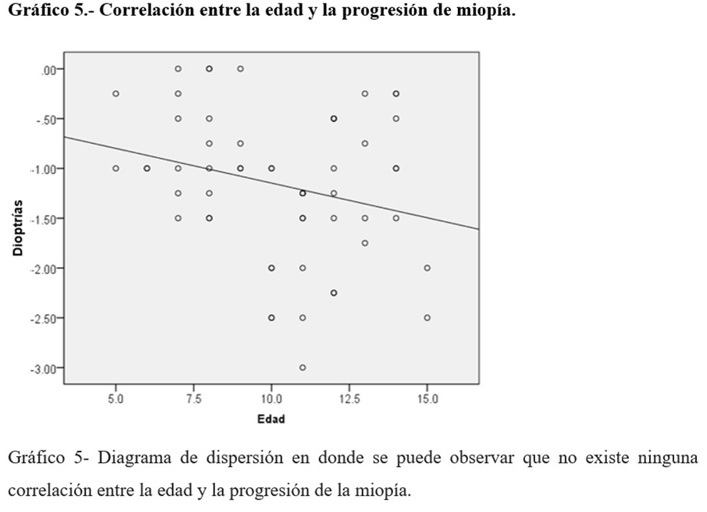
Se realizó un análisis para saber la relación que existe entre la edad y la progresión de la miopía durante el año de tratamiento con atropina al 0.01%. Se puede observar que no existe ninguna correlación entre dichas variables, por lo que la disminución de la progresión de la miopía no se relaciona con el grupo de edad. (p= 0.062). (Gráfico 5.)
DISCUSION
En este estudio se incluyeron a 28 pacientes del Hospital Civil de Culiacán, de 5 a 16 años, con una edad promedio de 10.21 años, los cuales recibieron una dilución de atropina al 0.01% durante un año como tratamiento para la progresión de la miopía leve y moderada, encontrando una diferencia tanto estadística como clínicamente significativa.
Se han propuesto diferentes opciones terapéuticas para el tratamiento de la miopía, como son el uso de diferentes tipos de lentes como son los lentes monofocales, bifocales, multifocales, lentes de contacto, la ortokeratologia, cirugía refractiva, así como medicamentos tópicos oftálmicos, por ejemplo, agentes muscarínicos e hipotensores oculares, sin embargo, ninguno de ellos ha probado ser eficaz para la disminución de la progresión de la miopía.
La atropina es el único medicamento que ha demostrado una eficacia frente a la progresión de la miopía en la población pediátrica presentando mínimos efectos adversos.
No se ha dilucidado el mecanismo exacto por el cual los agentes muscarínicos son eficaces para el tratamiento de la miopía, existen varias teorías, inicialmente se pensaba que la inhibición de la acomodación era un factor importante, sin embargo, estudios con animales se ha demostrado también una inhibición de la miopía, por lo que surge otra teoría, en donde la atropina puede tener efectos bioquímicos en la retina o la esclera, ya que existe un aumento de la exposición de luz ultravioleta secundario a la dilatación pupilar afectando el entrecruzamiento de las fibras de colágeno esclerales ya que inhiben la proliferación celular en los fibroblastos de la esclera en humanos y limitando así su crecimiento.7
Se han propuesto diferentes diluciones de atropina para demostrar la eficacia y seguridad para la progresión de la miopía en niños pediátricos. Inicialmente se propuso atropina 1%, 8 demostrando su efecto benéfico sobre la progresión de la miopía obteniendo una tasa de progresión en el primer año de -1.14±0.80 D sin embargo debido a los efectos adversos que presentaban los pacientes se han realizado otros estudios con diferentes tipos de diluciones, demostrando igualmente un efecto positivo sobre el equivalente esférico. Chia A, et al, propusieron diluciones de atropina al 0.5%, 0.01% y 0.01%, demostrando una progresión a los dos años de -0.30±0.60D, -0.38±0.60, -0.49±0.63 respectivamente4. Mas recientemente, Yam J et al, en el estudio LAMP (Low-Concentration Atropine for Myopia Progression Study), utilizaron concentraciones de atropina del 0.05%, 0.025% y 0.01%, demostrando una reducción de la progresión de miopía dependiente de la dosis a lo largo de un año, además de presentar mínimos efectos adversos.6
Existen diversos estudios que evidencian la eficacia y seguridad de la atropina al 0.01% la cual reduce la progresión de la miopía infantil, principalmente en la raza asiática, sin embargo, no está claro si las diferencias en la presentación y progresión de miopía en otros países podría estar asociado con una respuesta diferente a la dilución de atropina al 0.01%.(4) (5). Luke Larkin G, et al, realizaron un estudio de casos y controles multicéntrico y retrospectivo en donde se evaluaba la eficacia de la atropina al 0.01% durante dos años en una población que comprendía varios tipos de etnia (asiáticos, afro-americanos, americano-nativo etc); concluyendo el beneficio de la atropina en pacientes con miopía sin importar la raza. Hay evidencia de otras poblaciones en las cuales se demuestra la eficacia y seguridad de la atropina al 0.01%, como por ejemplo en Alemania y España. 5-9. Existe poca evidencia en la población mexicana sobre el tratamiento. En este estudio el 100% de los participantes son mexicanos.
Se cree que el alargamiento excesivo del globo ocular contribuye de manera importante a los cambios degenerativos de la miopía patológica. La atropina al 1% durante un año, ha demostrado que reduce la longitud axial de 0.09±0.19mm en comparación con el grupo placebo 0.70±0.63mm (p=0.004). (10). En el estudio de ATOM1, se analizaron cambios biométricos de 313 pacientes, los cuales incluyeron autorrefracción ciclopléjica, curvatura corneal, profundidad de la cámara anterior, grosor del cristalino y longitud axial; en los pacientes que tuvieron un efecto rebote por la suspensión del tratamiento de atropina 1%, se observó también un aumento de la profundidad de la cámara vitrea así como de la longitud axial (0.001). Por lo que se sugiere que uno de los efectos de la atropina es sobre estos dos últimos parámetros los cuales son importantes para la progresión de la miopía. 3
Fue hasta la realización del estudio ATOM 1 ( Atropine for the Tratment of Childhood Myopia) en donde se probó realmente la eficacia de la atropina como tratamiento para la progresión de la miopía, este estudio es un ensayo clínico controlado aleatorizado publicado en 2006 el cual incluyó un total de 400 niños chinos de 6 a 12 años, los cuales recibieron como intervención el fármaco atropina al 1% durante dos años, demostrando que es un tratamiento efectivo en el control de la miopía ya que la tasa de progresión de miopía es de -1.14 ±0.80 en un año, sin embargo, después de que el tratamiento es suspendido se observó un efecto rebote de la miopía, mostrando un aumento de la misma en el grupo de tratamiento, sin embargo, 3 años después de seguimiento, la progresión absoluta de miopía fue menor en el grupo de tratamiento con atropina al 1%. Además, una de las limitaciones de esta dilución son los efectos adversos como son dilatación pupilar, fotofobia, visión borrosa cercana, reportados en otros estudios.3
Consideramos como base el estudio ATOM2 11 el cual es un protocolo realizado en población pediátrica europea, en donde se comparó la media del equivalente esférico antes y después del tratamiento con atropina al 0.01%, concluyendo una tasa de progresión de miopía menor después del tratamiento durante un año, en nuestro estudio se inició la intervención en aquellos pacientes en los cuales había una tasa de progresión de miopía mayor a -0.50 D entre la refracción de la cita previa y la refracción actual, durante un periodo de doce meses.
Con la finalidad de reducir los efectos adversos reportados, se realizó el ATOM 2 en donde se compararon diferentes diluciones de atropina, 0.1%, 0.5% y 0.01% para la disminución de la progresión de la miopía, concluyendo que la dilución al 0.01% es la más efectiva a pesar el fenómeno de rebote después de la suspensión del mismo4. Por lo que en nuestro estudio no se realizó una aleatorización, por el contrario, se inició el tratamiento con la dilución de atropina al 0.01% en niños con una progresión de miopía de -0.50 D, obteniendo resultados estadística y clínicamente significativos, además de que solo se presentaron efectos adversos mínimos, 5 pacientes del total presentaron ardor ocular.
En nuestro estudio se demostró una disminución de la progresión de la miopía en la población pediátrica de -0.58 D con el uso de atropina al 0.01%, similar a lo que se concluyó en el estudio sobre la eficacia de atropina 0.01% para el tratamiento de la miopía infantil en pacientes europeos, en donde se comprobó la disminución de la progresión de la miopía de -0.54 D durante un año de tratamiento12.
Al realizar las comparaciones entre la última medición (mes 12) -4.95±-0.56 D, comparada con las tres mediciones previas encontramos diferencia estadísticamente significativa entre los dos primeros tiempos, es decir, al inicio y los 4 meses, p=0.000 y p=0.001 respectivamente, observándose una máxima mejoría al mes 8. No existe una diferencia significativa entre la comparación del mes 8 y el mes 12 (p=0.255) sin embargo hay una relevancia clínica ya que hay una reducción de 0.32 dioptrías.
En nuestro estudio se realizó el análisis de la progresión del astigmatismo a través del tiempo, se realizaron las mediciones al inicio -1.59±1.08, a los 4, 8 y 12 meses, -1.63±1.13D, -1.59 ±1.10D, -1.60±1.07D, teniendo una diferencia entre la primera medición y la última de -0.001 D, con una p=0.975.
La respuesta del efecto antimiópico de la atropina en sus diferentes diluciones, ha sido estudiada en diferentes grupos de edades. Similar con un estudio que se realizó en una población en Alemania, no observaron una correlación entre la edad y efecto de la terapia, en nuestra población tampoco se demostró una correlación entre la edad y la progresión de la miopía.(p=0.062).
CONCLUSION
El presente estudio demuestra que la atropina, además de ser un medicamento de bajo costo y buena disponibilidad, ayuda de manera eficaz al retraso de la miopía, esto dando un impacto positivo en el sentido clínico y económico como medida de salud pública, ya que se demostró una reducción de la progresión de la miopía de -0.58 D (p=0.05) en la población estudiada con atropina al 0,01% durante un año, desafortunadamente la falta de un grupo control en este estudio limita de manera importante la capacidad de evaluar el efecto de la atropina. En la actualidad se están realizando diversos estudios clínicos en diferentes partes del mundo para poder determinar diversas variables necesarias para evaluar la verdadera eficacia y seguridad a largo plazo de este medicamento en la miopía en los pacientes pediátricos.
AGRADECIMIENTOS
Con especial agradecimiento al Hospital Civil de Culiacán, CIDOCS, a mis maestros y compañeros.
REFERENCIAS